
某实验小组在实验室中制取氨气并设计实验验证氨气的某些性质。
(1)实验室制取氨气的化学方程式为______________________________,其装置与制取__________(填“H2”、“O2”或“CO2”)的装置相同,干燥氨气要用__________,检验氨气时可以用__________试纸。
(2)利用如下图所示的装置,可以验证NH3和HCl的有关性质。
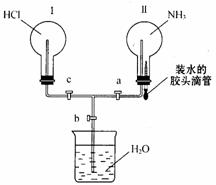
实验前a、b、c活塞均关闭。(已知HCl极易溶于水且能快速溶解。)
①若要在烧瓶II中产生“喷泉”现象,烧瓶I中不产生“喷泉”现象,其操作方法是________________________________________。
②若先打开a、c活塞,再挤压胶头滴管,在烧瓶II中可观察到的现象是__________。
③通过挤压胶头滴管和控制活塞的开关,在烧瓶I中产生“喷泉”现象,烧瓶II中不产生“喷泉”现象,其操作方法是________________________________________。
科目:高中化学 来源: 题型:阅读理解
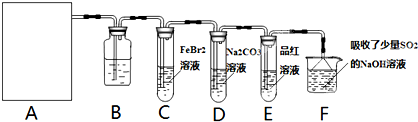
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
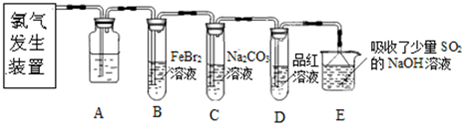
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4 | 14.3 | 20.7 | 28.5 | 40.0 | 55.0 | 75.4 |
| Cu(NO3)2 | 81.8 | 124.8 | 163.1 | 181.8 | 207.8 | 247.3 |
| 实验步骤 | 预期现象 |
| 步骤1:除铁.将铜粉置于烧杯中, |
|
| 步骤2:溶解.将步骤1得到的铜粉置于烧杯中, |
|
| 步骤3:结晶.将步骤2所得溶液蒸发浓缩至液面有晶膜出现,冷却至室温,过滤得粗产品. | / |
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组在实验室中制取氨气并设计实验验证氨气的某些性质:
(1)实验室制取氨气的化学方程式为_____________,其装置与制取_____________ (填“H2”“O2”或“CO2”)的装置相同,干燥氨气要用_____________,检验氨气时可以用_____________试纸.
(2)利用如下图所示的装置,可以验证NH3和HCl的有关性质.
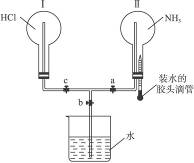
实验前a、b、c活塞均关闭.
①若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是:
_____________________________________________________________________________________________________________________________________________________________.
②若先打开a、c活塞,再挤压胶头滴管,在烧瓶Ⅱ中可观察到的现象是: .
③通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是_____________________________________________________________
若要在该装置中产生双喷泉现象,其操作方法是___________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com