
| A.工业上电解熔融AlCl3制取金属铝 |
| B.镁在空气中燃烧的产物只有MgO |
| C.海水提镁和海水提取溴所涉及的化学反应全部是氧化还原反应 |
| D.铜表面形成的铜绿的主要成分为Cu2(OH)2CO3 |
| ||
| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源:不详 题型:单选题
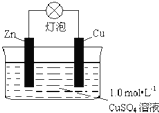
| A.负极反应为:Zn-2e-→Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2++Cu |
| C.电解质溶液中的SO42-移向Cu电极 |
| D.在外电路中,电子从Zn极流向Cu极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由Fe、Cu与稀硫酸溶液组成的原电池,其负极反应式为:Fe-3e-═Fe3+ |
| B.由Al、Mg与氢氧化钠溶液组成的原电池,其负极反应式为:Mg-2e-+2OH-═Mg(OH)2 |
| C.由Pb、Cu与氯化铁溶液组成的原电池,其正极反应式为:Cu-2e-═Cu2+ |
| D.由Al、Cu与浓硝酸组成的原电池,其负极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2Al+WO3
| ||||
B.2Ag2O
| ||||
C.3CO+Fe2O3
| ||||
D.2AlCl3(熔融)
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
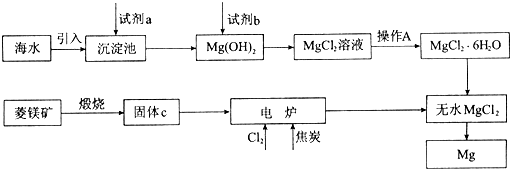
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
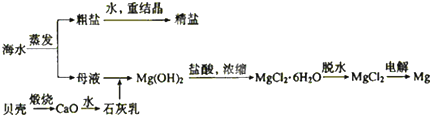
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.56 L | B.1.12 L | C.2.24 L | D.3.36 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2SO4 | B.AgNO3 | C.Na2SO4 | D.NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com