
 这4种微粒结构示意图,判断下列说法中正确的是( )
这4种微粒结构示意图,判断下列说法中正确的是( )| A. | 它们都带有电荷 | B. | 它们表示同一种元素 | ||
| C. | 它们核外电子排布相同 | D. | 它们都具有相对稳定结构 |
分析 根据核内质子数与核外电子数的关系分析微粒所带的电荷数;不同种元素之间的本质区别是质子数不同,通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构是一种稳定结构;进行解答.
解答 解:A、在第二个和第四个微粒中核内质子数等于核外电子数,呈中性,而其它两个都带有电荷,故A说法错误;
B、元素是质子数(即核电荷数)相同的一类原子的总称,由于微粒的质子数不同,不可能属于同一种元素,故B说法错误;
C、核外电子排布相同应该是电子层数和每一层上的电子数也相同,可以看出前三种微粒的核外电子排布是相同的,最后一个多了一个电子层,故C说法错误;
D、根据通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构是一种稳定结构,可知它们都具有相对稳定结构,故D说法正确;
故选:D.
点评 本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 除去CO2中的少量CO(点燃) | |
| B. | 验证硫酸铵溶液(取样,加氢氧化钠溶液) | |
| C. | 检验CaO中混有的CaCO3溶液(滴加稀盐酸) | |
| D. | 鉴别氢氧化钠和碳酸钠(取样,溶解,滴加酚酞) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | t2℃时,将50ga物质(不含结晶水)放入100g水中充分溶解得到a的饱和溶液 | |
| C. | 将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
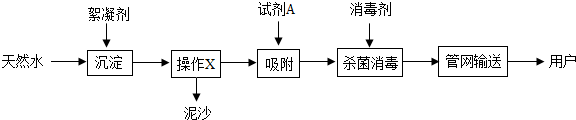
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 溶解度是解决溶液相关问题的重要依据.
溶解度是解决溶液相关问题的重要依据.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 100 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
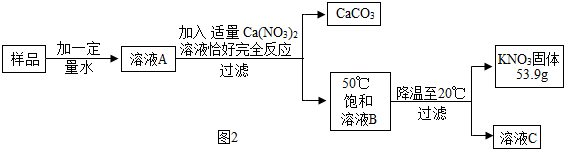
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.
A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲线如图.某学习小组对加入0~VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探究:
将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲线如图.某学习小组对加入0~VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤能除去天然水中所有的杂质 | |
| B. | 将活性炭放入硬水中可使其软化 | |
| C. | 工业废水要经过处理后再排放 | |
| D. | 过量使用农药、化肥不会造成水体污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com