
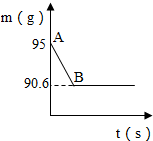
 鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:
鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中碳酸钙的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除碳酸钙外的其他成分不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所有盐酸刚好消耗了加入量的一半.试计算:| 14.6g |
| 80g |


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
化学与我们的生产、生活有着非常密切的联系,利用家庭生活中常见的物品也能进行很多化学探究活动。下面是小华利用家中相关物品进行的实验探究:
(1)小华将石蕊溶液分别滴入白醋和纯碱溶液中,发现石蕊在白醋中变红色,在纯碱溶液中变蓝色,说明白醋显酸性,纯碱溶液的pH__________7(填“大于”、“小于”或“等于”)。
(2)白醋的主要成分是醋酸,酸有很多相似的性质,如:①酸能使石蕊变红 ②酸能与活泼金属反应生成盐和氢气 ③酸能与碱反应生成盐和水 ④酸能与金属氧化物反应生成盐和水 ⑤酸能与碳酸盐反应生成盐、水和二氧化碳等。为什么不同的酸都具有相似化学性质?
小华将生锈的铁钉放在小玻璃杯中,加入白醋,发现_______ ,说明白醋能与铁锈反应。小华想到目前世界卫生组织正在推广使用中国铁锅,于是建议在使用铁锅做菜时放点醋,可以补充人体需要的微量元素铁元素,原因是__________(填序号);同时由于__________(填序号),他还认为可以用白醋来除去水壶中的水垢。
小华将白醋滴加到纯碱溶液中,发现溶液中有气泡产生,他认为酸碱发生中和反应时,生成了气态的水,请问:小华的认识正确吗?为什么?
(3)小华发现某食品包装中装有一小袋“生石灰干燥剂”,主要成分是氧化钙,他将此干燥剂放入水中,发现水的温度升高了,这是因为_____________________________________。
(4)小华经查阅材料得知,醋酸的化学式为CH3COOH,则醋酸中碳元素的质量分数为_______________。
(5)鸡蛋壳的主要成分是碳酸钙,小华将12.5g鸡蛋壳放入100g足量的食醋中,充分反应后剩余物质的质量为108.1g,请计算该鸡蛋壳中含有碳酸钙的质量分数是多少?【提示:2CH3COOH+CaCO3=Ca(CH3COO)2+H2O+CO2↑】
查看答案和解析>>
科目:初中化学 来源:2011-2012学年四川省成都市铁路中学九年级(下)月考化学试卷(2月份)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com