
科目:初中化学 来源: 题型:
| 小柯:实验测定法 | 小妍:计算法 | ||||
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL. | 解:高锰酸钾中氧元素的质量分数=
=
=40.5% 氧气的质量为15.8g×40.5%=6.4g 答:15.8g高锰酸钾完全分解产生氧气6.4g. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 操作步骤和实验现象 | 简 答 |
| ①取16克氧化铜和2克炭粉均匀混合,放入质量为48.2克的B玻璃管中. | 请写出装置中仪器的名称: 甲 酒精灯 酒精灯 、乙铁架台 铁架台 丙集气瓶 集气瓶 .B玻璃管和氧化铜、炭粉的总质量为66.2g 66.2g . |
| ②仪器:打开弹簧夹,往储气瓶中注入水. | 水应从 d d 通入(填接口编号,见上图),仪器的连接顺序应是:e e 接b(或c) b(或c) :c(或b) c(或b) 接a a . |
| ③先通入一段时间纯净、干燥的氮气. | 其目的是: 排尽玻璃管内空气 排尽玻璃管内空气 |
| ④夹紧弹簧夹后,加热氧化铜,可看到B玻璃管内的固体逐渐由黑色变为红色 | 要验证假设,A瓶中应装的液体是: 足量澄清的石灰水 足量澄清的石灰水 ,它的作用是:检验生成的气体是二氧化碳,并吸收 检验生成的气体是二氧化碳,并吸收 . |
| ⑤实验完毕后,冷却到室温,称B玻璃管和固体总质量为64.8克,称A瓶连液体增重1.2克. | B玻璃管连固体减少的质量 大于 大于 (填大于或小于或等于)A瓶连液体增加的质量. |
| 结论:根据数据处理结果,得出原假设 不成立 不成立 . | |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
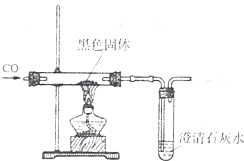 (2008?遵义)碱式碳酸铜[化学式Cu2(OH)2CO3,相对分子质量为222]加热完全分解后生成的黑色固体是什么?甲、乙、丙、丁四位同学对此进行探究.请你与他们一起,踏上探究之路.
(2008?遵义)碱式碳酸铜[化学式Cu2(OH)2CO3,相对分子质量为222]加热完全分解后生成的黑色固体是什么?甲、乙、丙、丁四位同学对此进行探究.请你与他们一起,踏上探究之路.| 12 |
| 222 |
| 12 |
| 222 |
| 222 |
| 2.5g |
| 2×80 |
| x |
| 2×64 |
| 222 |
| 64 |
| 80 |
| 222 |
| 2.5g |
| 2×80 |
| x |
| 2×64 |
| 222 |
| 64 |
| 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 研究性学习小组对炭粉与氧化铜反应产物中的气体成分进行研究:
研究性学习小组对炭粉与氧化铜反应产物中的气体成分进行研究:| 操作步骤和实验现象 | 简 答 |
| ①称取16克氧化铜和2克炭粉均匀混合,放入质量为48.2克的B玻璃管中. | 玻璃管与药品的总质量是 66.2 66.2 克. |
| ②连接上述仪器,先通入一段时间纯净、干燥的氮气后,加热氧化铜. | 可看到B玻璃管内现象为 固体黑色变红色 固体黑色变红色 . |
| ③实验完毕后,冷却到室温,称B玻璃管和固体总质量为64.8克,称A瓶连液体增重1.2克. | B玻璃管连固体减少的质量 大于 大于 (填大于或小于或等于)A瓶连液体增加的质量. |
| 结论:根据数据处理结果,得出原假设 不成立 不成立 . | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com