
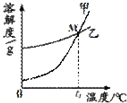
 (1)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如图.
(1)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如图.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |


科目:初中化学 来源: 题型:阅读理解
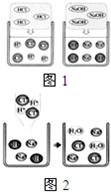 (2011?乌鲁木齐)在高效复习课堂中,同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾”四种物质的溶液对“复分解反应发生的条件”进行再探究.
(2011?乌鲁木齐)在高效复习课堂中,同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾”四种物质的溶液对“复分解反应发生的条件”进行再探究.查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验方案 | 实验现象 | 实验结论 |
| 酚酞试液变红与CO32-有关. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
可能含SO42- 可能含SO42- |
取上述溶液少量于试管中,加入少量硝酸钡溶液.若出现白色沉淀,则说明含有SO42-;若没有出现白色沉淀,则说明上述溶液中不含有SO42-. 取上述溶液少量于试管中,加入少量硝酸钡溶液.若出现白色沉淀,则说明含有SO42-;若没有出现白色沉淀,则说明上述溶液中不含有SO42-. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 预期现象和结论 |
| 步骤1: 取少量的澄清滤液于试管中,然后向其中加入足量的硝酸钡溶液, 取少量的澄清滤液于试管中,然后向其中加入足量的硝酸钡溶液, |
①若产生白色沉淀,则含有碳酸钾; ②若无明显现象,则猜想④不正确; ①若产生白色沉淀,则含有碳酸钾; ②若无明显现象,则猜想④不正确; |
| 步骤2: 将步骤1中的溶液静置,然后取上层清液于试管中,然后向其中滴加酚酞试液 将步骤1中的溶液静置,然后取上层清液于试管中,然后向其中滴加酚酞试液 |
①若溶液变为红色,则含有氢氧化钾; ②若溶液不变色说明猜想④不正确; ①若溶液变为红色,则含有氢氧化钾; ②若溶液不变色说明猜想④不正确; |
查看答案和解析>>
科目:初中化学 来源:2011年天津市河西区九年级结课考试化学试卷(解析版) 题型:解答题
| 实验操作 | 预期现象和结论 |
| 步骤1:______ | ______ |
| 步骤2:______ | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com