
| 实验操作 | 现 象 | 结 论 |
| ________ | ________ | 猜想①成立 |
| ________ | ________ | 猜想②成立 |
| ________ | ________ | 猜想③成立 |
| 实验操作 | 现 象 | 结 论 |
| 取少量固体物质于试管中,加入足量稀盐酸 | 固体不溶解,溶液呈无色 | 猜想①成立 |
| 取少量固体物质于试管中,加入足量稀盐酸 | 固体部分溶解,溶液呈蓝色 | 猜想②成立 |
| 取少量固体物质于试管中,加入足量稀盐酸 | 固体部分溶解,有气体产生,溶液呈无色 | 猜想③成立 |


科目:初中化学 来源: 题型:
| 实验操作 | 现 象 | 结 论 |
取少量固体物质于试管中,加入足量稀盐酸 取少量固体物质于试管中,加入足量稀盐酸 |
固体不溶解,溶液呈无色 固体不溶解,溶液呈无色 |
猜想①成立 |
取少量固体物质于试管中,加入足量稀盐酸 取少量固体物质于试管中,加入足量稀盐酸 |
固体部分溶解,溶液呈蓝色 固体部分溶解,溶液呈蓝色 |
猜想②成立 |
取少量固体物质于试管中,加入足量稀盐酸 取少量固体物质于试管中,加入足量稀盐酸 |
固体部分溶解,有气体产生,溶液呈无色 固体部分溶解,有气体产生,溶液呈无色 |
猜想③成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.
碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成.
| ||
| ||
| 12 |
| 222 |
| 12 |
| 222 |
| 物 质 | H2SO4 | Na2SO4 | MgSO4 |
| 常温下的溶解度∕g | 与水以任意比互溶 | 18.0 | 39.0 |
查看答案和解析>>
科目:初中化学 来源:2006年贵州省黔南州都匀市中考化学试卷(课标卷)(解析版) 题型:解答题
| 实验操作 | 现 象 | 结 论 |
| ______ | ______ | 猜想①成立 |
| ______ | ______ | 猜想②成立 |
| ______ | ______ | 猜想③成立 |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年广东省珠海市九年级第三次模拟考试化学试卷(解析版) 题型:探究题
碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成。
(1)提出问题: 黑色固体是什么?
(2)猜想与假设: 黑色固体可能是:① ;②可能是炭粉;③可能是炭粉和氧化铜的混合物。请你补充猜想①。作出这些猜想的依据是 。
(3)实验方案: 他们称取了2.22g碱式碳酸铜在试管中高温加热使之完全分解,冷却至室温,称得黑色固体产物的质量为1.6g。
(4)实验反思:① 甲同学经过思考后,认为可以排除猜想③,理由是 (用化学方程式表示)。
② 乙同学根据质量守恒定律:化学反应前后,元素的种类和质量都不变。通过对得到的数据进行计算,排除了猜想②,他的理由是(通过计算式说明) 。
(5)实验结论:结合甲、乙同学的探究和查阅资料,丙同学确认只有猜想①成立。
(6)实验拓展:丙同学想进一步探究该黑色固体的化学性质。他发现实验室有一瓶无色溶液,其标签严重破损(如图),
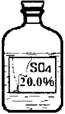
老师告诉他该瓶试剂是硫酸、硫酸钠或硫酸镁溶液中的一种。他通过查阅资料得知常温下这三种物质的溶解度如下表:
|
物 质 |
H2SO4 |
Na2SO4 |
MgSO4 |
|
常温下的溶解度∕g |
与水以任意比互溶 |
18.0 |
39.0 |
丙同学根据以上信息,分析此溶液一定不是 溶液。为确定其成分,他取了少量黑色固体放入试管中,然后向其中滴加了一定量的该无色溶液后,发现黑色固体全部消失,溶液由无色变为蓝色。他确定该溶液为 。其反应的化学方程式为 。
【解析】初中阶段常见的黑色物质有:氧化铜、碳、二氧化锰、四氧化三铁等.然后根据化学反应前后元素种类不变,进行分析确定物质组成,(4)①碳具有还原性,能够和金属氧化物发生氧化还原反应,所以碳和氧化铜不能同时存在,②2.22g碱式碳酸铜含碳元素的质量为12/222×22.2g=0.12g≠1.6g,
(6)由标签可知:溶液的质量分数是20%,题中给出三种物种的溶解度,根据溶解度计算,在该温度下,饱和溶液中的溶质的质量分数,分析不可能的是什么.可能是什么;硫酸铜溶液是蓝色的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com