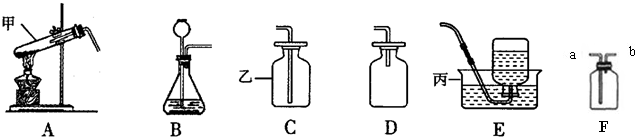
解:(1)指定仪器是试管和集气瓶;
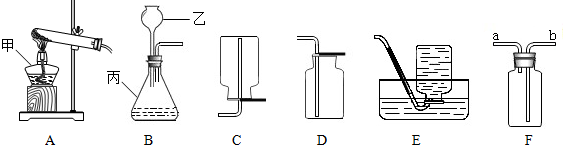
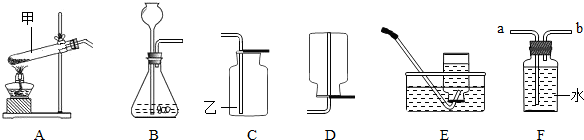
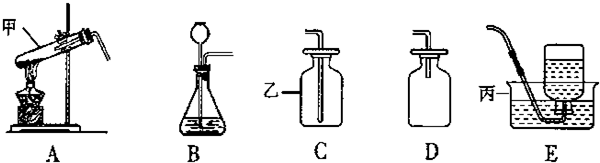
(2)加热高锰酸钾固体制取氧气,试管口应低于试管底部,防止冷凝水倒流引起试管炸裂,试管口要放一团棉花,防止高锰酸钾粉末进入导管;高锰酸钾加热生成氧气的同时还生成锰酸钾、二氧化锰和氧气,反应的表达式是:高锰酸钾

锰酸钾+二氧化锰+氧气,该反应由一种物质分解生成三种物质,属于分解反应;用排水法收集氧气时,要等集气瓶口气泡连续、均匀冒出再开始收集,防止收集的氧气不纯;实验完毕,要先移导管后熄灯,防止水倒吸引起试管炸裂;若收集的氧气不纯,可能是瓶内未装满水,或导管口有气体生成就立即收集;
(3)用过氧化氢溶液制取并收集一瓶较为干燥的氧气,不需加热,属于固液常温型,氧气的密度比空气大,故要制取干燥的氧气可用向上排空气法;实验开始前要检查装置气密性,防止装置漏气;可将带火星的木条放于集气瓶口,观察木条是否复燃进行验满;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应表达式是:过氧化氢
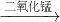
水+氧气;
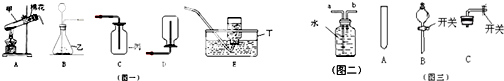
(4)氧气的密度比水小,所以应从b导管进入,随着氧气的增多,将水挤压到集气瓶底部通过a导管排尽;
(5)实验验证:实验一:根据实验现象是木条不复燃,说明了是用木条在检验是否生成了氧气,对比实验二的操作,可以得出实验一的操作;
实验二:根据实验现象:木条复燃,说明了氧气的存在,更说明加入水泥块后过氧化氢中有较多氧气产生;
讨论与反思:研究是否是催化剂不但要从能够改变反应速率方面分析.还要从反应前后质量不变方面进行分析;
实验步骤:水泥块是从溶液中取出的,要得到水泥块的质量,就需要将水泥中的水分除去,然后用天平称量质量才能比较反应前后质量是否改变;
研究催化剂,除了研究改变反应速率,反应前后质量不变,还要研究反应前后的化学性质不变;
故答案为:(1)试管;集气瓶;
(2)试管口高于试管底部(或试管口未放棉花);试管口应低于试管底部(或在试管口放一团棉花);冷凝水倒流引起试管炸裂(加热时高锰酸钾粉末进入导管);高锰酸钾

锰酸钾+二氧化锰+氧气;分解;集气瓶口有气泡冒出;移导管;熄灯;集气瓶内未装满水(或集气瓶口有气泡就立即收集);
(3)B;C;检查装置的气密性;氧气的密度比空气大;将带火星的木条放于瓶口,若木条复燃则满;过氧化氢
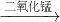
水+氧气;
(4)实验验证:
| | 实验步骤 | 实验现象 | 实验结论 |
| 实验一 | 将带火星的木条伸入盛有过氧化氢的试管中 | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢的分解速率 |
讨论与反思:水泥块在反应前后质量是否改变;
实验步骤:干燥;称量;水泥块的化学性质在反应前后是否改变.
分析:(1)依据常用仪器回答;
(2)根据高锰酸钾制取氧气的实验注意事项、反应原理、反应特点等分析回答;
(3)用过氧化氢溶液制取并收集一瓶较为干燥的氧气,不需加热,属于固液常温型,要制取干燥的氧气可用排空气法,然后依据氧气的密度、过氧化氢分解的反应原理、氧气的助燃性分析解答;
(4)氧气的密度比水小;
(5)实验验证:实验一:根据氧气具有助燃性进行分析;
实验二:根据木条复燃的现象分析,说明水泥块有催化作用;
讨论与反思:根据催化剂的定义分析需要验证的因素,
实验步骤:根据洗涤后的固体中含有水分进行分析,并称量洗涤后固体质量;然后根据催化剂满足还需的条件分析.
点评:本题对于实验室制取氧气的反应原理、实验注意事项、装置选取等知识进行了综合考查,在研究催化剂时,要从改变反应速率、反应前后的质量、化学性质等方面进行研究.

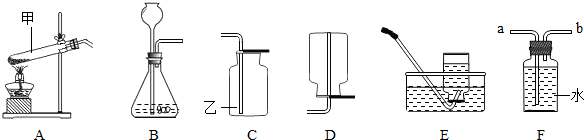
 锰酸钾+二氧化锰+氧气,该反应由一种物质分解生成三种物质,属于分解反应;用排水法收集氧气时,要等集气瓶口气泡连续、均匀冒出再开始收集,防止收集的氧气不纯;实验完毕,要先移导管后熄灯,防止水倒吸引起试管炸裂;若收集的氧气不纯,可能是瓶内未装满水,或导管口有气体生成就立即收集;
锰酸钾+二氧化锰+氧气,该反应由一种物质分解生成三种物质,属于分解反应;用排水法收集氧气时,要等集气瓶口气泡连续、均匀冒出再开始收集,防止收集的氧气不纯;实验完毕,要先移导管后熄灯,防止水倒吸引起试管炸裂;若收集的氧气不纯,可能是瓶内未装满水,或导管口有气体生成就立即收集;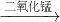 水+氧气;
水+氧气; 锰酸钾+二氧化锰+氧气;分解;集气瓶口有气泡冒出;移导管;熄灯;集气瓶内未装满水(或集气瓶口有气泡就立即收集);
锰酸钾+二氧化锰+氧气;分解;集气瓶口有气泡冒出;移导管;熄灯;集气瓶内未装满水(或集气瓶口有气泡就立即收集);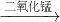 水+氧气;
水+氧气;

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案