
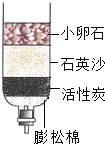
 (2007?常德)某校化学兴趣小组对学校池塘的水质状况开展了一系列的实验与研究.下面是同学们的部分实验内容,请参与他们的研究并回答下列问题:
(2007?常德)某校化学兴趣小组对学校池塘的水质状况开展了一系列的实验与研究.下面是同学们的部分实验内容,请参与他们的研究并回答下列问题:

科目:初中化学 来源: 题型:
 (2007?常德)据有关部门统计:每年全世界因生锈损失的钢铁约占钢铁年产量的四分之一.为此,某同学对铁钉锈蚀的条件产生了研究兴趣,并设计了如图所示的实验.据此请回答以下问题:
(2007?常德)据有关部门统计:每年全世界因生锈损失的钢铁约占钢铁年产量的四分之一.为此,某同学对铁钉锈蚀的条件产生了研究兴趣,并设计了如图所示的实验.据此请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 (2007?常德)某同学为了研究影响金属与酸反应速率的因素,进行了一系列的探究实验.实验结果如图所示,图中每条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中的信息我们可以分析出影响金属与酸反应速率的因素有:
(2007?常德)某同学为了研究影响金属与酸反应速率的因素,进行了一系列的探究实验.实验结果如图所示,图中每条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中的信息我们可以分析出影响金属与酸反应速率的因素有:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
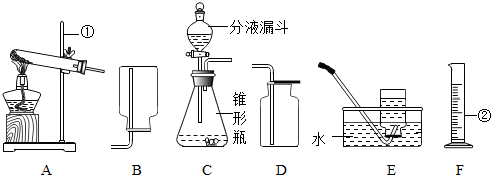
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2007?常德)常德市汉寿县是全国最大的淡水珍珠养殖县.为探究珍珠的化学成分,小明利用Google搜索引擎在互联网上查询得知:
(2007?常德)常德市汉寿县是全国最大的淡水珍珠养殖县.为探究珍珠的化学成分,小明利用Google搜索引擎在互联网上查询得知:| 实验步骤 | 主要实验现象 | 分步实验结论 |
| ①向珍珠粉样品中加入适 量的稀盐酸 |
试管 I中有气泡产生; 试管 II中的澄清石灰水变浑浊. |
珍珠粉样品中含有 碳酸根离子 碳酸根离子 |
| ②向反应后的试管 I的溶液 中滴加 碳酸钠 碳酸钠 溶液 |
试管 I中产生大量白色沉淀. | 珍珠粉样品中含有Ca2+ |
| 小明的实验结论是: 珍珠中含有碳酸钙 珍珠中含有碳酸钙 . | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com