
【题目】工业制备蔗糖的流程如下图所示。

(1)操作A名称是________,实验室进行操作C应在________(填仪器名称)中进行加热。
(2)糖汁呈棕黄色,工业上可加入________对糖汁进行脱色处理。
(3)关于工业制备蔗糖,下列说法正确的是________(选填序号)。
a.由甘蔗制得蔗糖的整个过程中主要是物理变化
b.操作A、C都要用到玻璃棒,其作用不同
c.为得到更多的蔗糖固体,进行操作C时应将水分蒸干再停止加热
【答案】过滤 蒸发皿 活性炭 ab
【解析】
(1)经过操作A得到糖汁(液体)和蔗渣(固体),过滤能将液体与固体分离,所以操作A名称是过滤,操作C是蒸发,实验室进行操作C应在蒸发皿中进行加热;
(2)活性炭具有吸附性,能吸附色素和异味,糖汁呈棕黄色,工业上可加入活性炭对糖汁进行脱色处理;
(3)a、根据流程图可知,由甘蔗制得蔗糖的整个过程中没有新物质生成,主要是物理变化,故a正确;b、操作A过滤,要用玻璃棒引流,操作蒸发要用玻璃棒搅拌,使液体均匀受热,所以操作A、C都要用到玻璃棒,其作用不同,故b正确;c、蒸发时出现多量固体应停止加热,利用蒸发皿的余热,使水分全部蒸发,故c错误,故选ab。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】水是生命之源,也是人类最宝贵的资源。小明同学将浑浊的河水倒入烧杯中,先加入明矾搅拌溶解,静置一会后,用图1所示的装置进行过滤,请问:
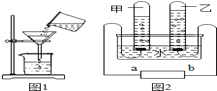
(1)图1装置中还缺少的一种仪器_______,该仪器的作用是____________。
(2)过滤后发现,滤液仍浑浊,可能的原因是__________。 (一种即可)
(3)改进后过滤,得到了澄清透明的水,用__________可判断水是硬水还是软水。
(4)消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为_______价。
(5)生活中常用_______ 的方法,既可降低水的硬度,又能消毒杀菌。
(6)利用图2所示的装置探究水的组成,写出该反应的符号表达式________,通电一段时间后,正极与负极产生气体的体积比约是_______,但在实验中所得数据略小于该值。针对这一现象,你认为可能的原因是__________。
A.实验所得数据与理论值相差不多,可认为实验已经成功
B.相同条件下,在水中溶解的氧气比氢气稍多
C.连接生成氧气一端的电极被氧气氧化,消耗了一部分氧气
(7)为了探究水电解的微观过程,小明同学做了一些分子、原子的模型,其中能保持氢气化学性质的粒子模型是_______。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. 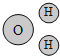
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组在学习氧气的化学性质时发现,铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰,该小组进行如下的探究:
(1)写出铁丝燃烧的文字表达式:__________
(2)探究 一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生如图所示);
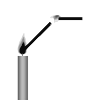
由此可知:蜡烛燃烧产生的火焰是由_______(填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 沸点/℃ | 燃烧时的温度/℃ | 是否有火焰 |
石蜡 | 300~550 | 约600 | 有 |
硫 | 444 | 暂无数据 | 有 |
铁 | 2750 | 约1800 | 无 |
钠 | 883 | 约1400 | 待测 |
①通过分析上表的数据,你认为物质燃烧时,什么情况下能产生火焰: ______;
②请推测金属钠在燃烧时________(填“有”或“无”)火焰产生
③表中硫的燃烧时温度是“暂无数据”,你认为合理的是___________(填编号)
A、200 B、300 C、400 D、800
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】牛奶是我们日常生活中一种营养丰富的饮品,每天饮用水可补充人们对钙等营养物质的需求.其中营养成分的具体含量如表所示.
请根据资料回答下列问题:
(1)牛奶中的钙主要以磷酸钙[ Ca3(PO4)2 ]的形式存在,磷酸钙中磷元素的化合价为_______。
(2)磷酸钙中钙、磷、氧三种元素的质量比为_____,磷酸钙中钙元素的质量分数为____(计算结果保留至 0.1%)
(3)乳酸钙(CaC6H10O6)是一种常见的补钙剂,乳酸钙片每片含乳酸钙436mg,通常中学生每天需从牛奶中补充550mg的钙元素,若只用乳酸钙片补钙,则理论上每天应服_____片乳酸钙片。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某某学习小组的同学对过氧化氢分解进行探究。
Ⅰ.(探究一)影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
实验序号 | H2O2溶液的溶质质量分数% | 温度℃ | MnO2粉末用量/g | 反应时间 |
① | 30 | 35 | 0 | t1 |
② | 30 | 55 | 0 | t2 |
③ | 5 | 20 | 0.1 | 3s |
④ | 15 | 20 | 0.1 | 1s |
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1______t2(填“>”“=”“<”)
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是_____(填实验序号),合理的结论是__________。
(交流探讨)MnO2属于金属氧化物,其它金属氧化物能否起到类似MnO2的催化作用?
Ⅱ、(探究二)探究Fe2O3是否对过氧化氢分解起催化作用
操作步骤 | 实验情况记录 | 结论 | |
① |
| A试管上方带火星的木条未复燃 B中出现气泡快,带火星的木条复燃 | Fe2O3_____(填“不影响”、“减慢”或“加快”)过氧化氢分解 |
② | 将B试管中的混合物过滤,把滤渣烘干、_____。 | 固体质量0.2g | Fe2O3质量未变 |
小组的同学认为要证明Fe2O3是催化剂,上述二个实验还不够,还需要再增加一个实验,
a、该实验的目的是:____________
b、请你设计实验证明,简要的写出实验步骤及实验现象:_________。
(得出结论)过氧化氢分解快慢受温度、浓度、催化剂等因素影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】地质考察人员发现一种带螺纹的矿石,研究时发现该矿石能在氧气中燃烧,主要反应是4X+11O2![]() Fe2O3+8SO2。下列有关说法中不正确的是
Fe2O3+8SO2。下列有关说法中不正确的是
A.X的化学式是FeS2 B.SO2中的硫、氧元素的个数比为1:2
C.反应前后氧元素的化合价发生改变 D.Fe2O3中铁元素的质量分数为70%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“氧循环”、“水循环”和“碳循环”是三大重要循环。
(1)自然界“氧循环”过程中消耗氧气的主要途径是动植物的呼吸和________。
(2)自然界“水循环”的主要变化过程与另外两种循环有本质的区别,从微观角度看,主要原因是:___________。
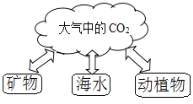
(3)自然界“碳循环”的部分循环途径如图所示。
①含碳单质的矿物燃烧的符号表达式为_______;
②海水吸收CO2反应的符号表达式是_________;该反应与绿色植物吸收CO2相比,反应物相同而产物不同的原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。
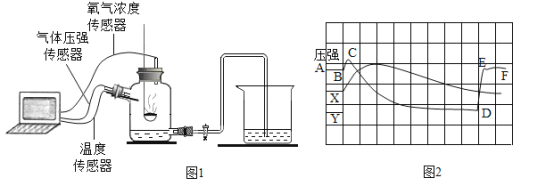
(1)红磷燃烧的化学方程式为 __;
(2)X曲线表示的是 _____(填“温度”或“氧气的浓度”);
(3)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_____ ;
(4)实验中测得的数据如下:
测量 项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 瓶中剩余气体的体积 | |
体积/mL | 80.0 | 46.4 | 126.0 |
根据实验数据计算:测得的空气中氧气的体积分数为______(列出计算式即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究表明Al3+在人体内会阻止小肠壁对磷的吸收,使血液和其它组织内磷的含量减少,造成记忆力减退,免疫功能下降,被世界卫生组织确定为食品污染源之一。营养学家指出每天铝的安全摄入量为每1千克体重0.7 mg(1 g = 1000 mg))。传统食品加工过程中。一般在1kg面粉中加入1g明矾(已知:明矾的化学式为KAl(SO4)2·12H2O,其相对分子质量是474)。请回答下列问题:
(1)1g明矾中含铝元素_______mg。
(2)该200g食品中含铝元素__________ mg 。
(3)体重为50 kg的某同学,一天用该食品200g,他摄入的铝量_______(选填“已”或“未”)超过安全摄入量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com