
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 0.9%NaCl溶液(ml) | 0.9%CuSO4溶液(ml) | 唾液溶液(ml) | 加入碘液3滴后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝色 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝色 |
分析 【实验结论】根据表格数据来分析;
【分析与交流】(1)根据酶在哪一温度下,催化效果最佳来分析;
(2)根据酶的组成和性质来分析;
(3)根据控制变量分析.
解答 解:【实验结论】根据实验结果酶的催化作用 受到重金属离子的影响;故填:会受到重金属离子的影响;
【分析与交流】
(1)因为37℃时酶的活性最强,所以将三只试管分别放入37℃的水浴;故填:37℃时酶的活性最强;
(2)酶是一种具有生命活性的蛋白质,故填:蛋白质;
(3)实验中盐用的是NaCl溶液和CuSO4溶液,除了金属离子不同,酸根离子也不同,可以将将实验中的CuSO4溶液更换成CuCl2溶液或将NaCl溶液换成Na2SO4溶液;
故填:甲、乙.
点评 本题考查蛋白质的性质,题目难度不大,了解中毒原理、或事故发生原因,才会正确对事故进行处理,保障人的生命安全.


科目:初中化学 来源: 题型:选择题
| A. | 氧化物中含有氧元素,所以含氧元素的化合物一定是氧化物 | |
| B. | 饱和溶液不能继续溶解某种溶质,则饱和溶液也不能继续溶解其他溶质 | |
| C. | 盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐 | |
| D. | 在金属活动性顺序里,位于氢前面的金属能置换出盐酸中的氢,所以铅能与盐酸反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
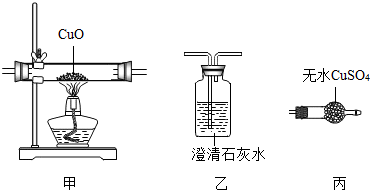
| A. | 甲、乙、丙 | B. | 丙、乙、甲 | C. | 丙、甲、乙、丙 | D. | 丙、甲、丙、乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.
碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.| 钙片质量 | 空洗气瓶质量 | 澄清石灰水的质量 | 反应后洗气瓶及瓶内物质总质量 |
| 25g | 100g | 200g | 300.4g |
| 加入稀盐酸的质量 | 100g | 200g | 300g | 400g |
| 充分反应后烧杯及杯内物质总质量 | 222.8g | 320.6g | 418.4g | 518.4g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某白色固体溶于水放热,该固体一定是生石灰 | |
| B. | 燃着的木条伸入瓶中熄灭,则瓶中一定不含氧气 | |
| C. | 盐酸与一种固体反应产生气泡,该固体一定是碳酸盐 | |
| D. | 能使无色酚酞溶液变红的一定是碱性溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com