
| ||
| ||
| ||



 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源:2013-2014北京市朝阳区2014年中考一模化学试卷(解析版) 题型:探究题
(7分) 据报道,一辆载满20t电石的货车,在高速路上发生意外,燃起大火并伴有大量黑烟,这辆货车在雨中燃烧了很长时间。某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动。
【查阅资料】①碳化钙与水反应生成一种可燃性气体和一种白色固体。
②乙炔(C2H2)气体燃烧时伴有大量黑烟。
【猜想假设】甲同学对碳化钙与水反应的生成物作出如下猜想:
可燃性气体可能是:①氢气 ②氧气 ③乙炔
白色固体可能是: ①氧化钙 ②氢氧化钙 ③碳酸钙
(1)你认为甲同学猜想的理由是 。
(2)其他同学讨论后认为甲同学的猜想有不合理之处,请指出并说明理由
。
【实验探究】
步骤1:取适量碳化钙加水,收集生成的气体,验纯后点燃,气体燃烧,伴有大量黑烟,说明碳化钙与水反应产生的气体是 。
步骤2:取适量反应后生成的固体于试管中, ,说明碳化钙与水反应产生的固体是氢氧化钙。
【反思交流】
(1)碳化钙与水反应的化学方程式为 。
(2)下列说法正确的是 (填字母序号)。
A.碳化钙与水反应放热
B.碳化钙应贮存在阴凉干燥的库房
C.碳化钙与水反应可用于测定电石中碳化钙的含量
D.实验室用电石与水制乙炔的发生装置与制氧气完全相同
查看答案和解析>>
科目:初中化学 来源:2013-2014北京市朝阳区2014年中考一模化学试卷(解析版) 题型:选择题
从分子的角度分析,下列解释不正确的是
A.水结冰体积变大——分子大小发生改变
B.氧气加压后贮存在钢瓶中——分子间有间隔
C.水通电生成氢气和氧气——分子在化学变化中可分
D.湿衣服在太阳下干得快——分子运动速率与温度有关
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.金刚石是一种单质 |
| B.该反应中生成了新的原子 |
| C.碳是非金属元素 |
| D.该反应是置换反应 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
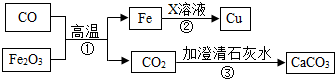
| A.反应①中Fe2O3发生还原反应 |
| B.反应②的化学方程式是:Fe+Cu(OH)2═Cu+Fe(OH)2 |
| C.X溶液可能是氯化铜溶液 |
| D.反应③可以检验二氧化碳气体 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

| ||
| 物质 | H2 | N2 | O2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com