
 某化学兴趣小组展示了他们设计的“火龙生字”创新实验,用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体如图1所示.用带火星的木条接触硝酸钾晶体,立即有火花出现,并缓慢地沿着字的笔迹蔓延,最后呈现出“火”字的黑色痕迹(如图2).现场的同学对此产生了浓厚的兴趣,随后进行了如下研究:
某化学兴趣小组展示了他们设计的“火龙生字”创新实验,用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体如图1所示.用带火星的木条接触硝酸钾晶体,立即有火花出现,并缓慢地沿着字的笔迹蔓延,最后呈现出“火”字的黑色痕迹(如图2).现场的同学对此产生了浓厚的兴趣,随后进行了如下研究:| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
分析 根据已有的知识进行分析,化学反应前后元素的种类不变;要证明生成了氧气,可以使用带火星的木条进行检验;促进燃烧可以增大氧气的浓度;根据硝酸钾的溶解度进行分析解答.
解答 解:【猜想与假设】:二氧化氮不是单质,而硝酸钾中不含有氢元素,不可能生成氢气.
故为:二氧化氮不是单质,硝酸钾中不含有氢元素;
【进行实验】:要证明生成氧气,可以取硝酸钾晶体放在试管中加热,然后将带火星的木条伸进试管内,观察到木条复燃,证明生成的是氧气;
故为:将少量硝酸钾晶体放在试管中加热,把带火星的木条放在试管中;木条复燃;2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2+O2↑;
【解释与结论】:促进燃烧可以增大氧气的浓度,白纸上写过字的地方更容易燃烧的原因是硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大;
故为:硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大;
【反思与评价】:根据表格可以看出,硝酸钾的溶解度随温度的升高而增大,使用“硝酸钾的热饱和溶液”书写文字,可以使更多的硝酸钾晶体附着在白纸表面.
故为:硝酸钾的溶解度较大,用热饱和溶液能使白纸上附着更多的硝酸钾晶体
故答案为:【猜想假设】二氧化氮不是单质 硝酸钾中不含氢元素
【进行实验】将少量硝酸钾晶体放入试管中加热,把带火星的木条伸入试管中
带火星的木条复燃 2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2+O2↑
【解释与结论】硝酸钾晶体受热生成氧气,使得写过字的白纸附近氧气浓度增大;
【反思与评价】硝酸钾的溶解度随温度的升高而增大,用热饱和溶液能使白纸上附着更多的硝酸钾晶体.
点评 本题考查了化学实验的设计以及溶解度的知识,完成此题,可以依据已有的知识进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用熟石灰制生石灰 CaO+H2O=Ca(OH)2 化合反应 | |
| B. | 用氯酸钾和二氧化锰制取氧气 2KC1O3$\frac{\underline{MnO_2}}{△}$2KC1+3O2↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
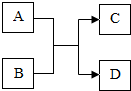 A、B、C、D都是初中化学中常见的物质,A、C为组成元素相同的两种气体氧化物,D为紫红色金属单质.它们之间的相互转化关系如图(图中反应条件已略去).则:
A、B、C、D都是初中化学中常见的物质,A、C为组成元素相同的两种气体氧化物,D为紫红色金属单质.它们之间的相互转化关系如图(图中反应条件已略去).则:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO〔CO2〕-通过灼热的氧化铜 | B. | NaOH〔Ca(OH)2〕-加入氯化钙溶液 | ||
| C. | CaCO3固体〔CaO固体〕-高温煅烧 | D. | Cu粉〔Fe屑〕-磁铁分离 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
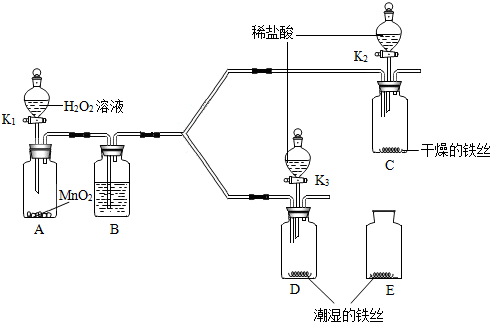
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
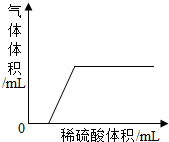 取HCl、NaOH、Na2CO3、CaCl2四种溶液中的任意两种混合.
取HCl、NaOH、Na2CO3、CaCl2四种溶液中的任意两种混合.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com