
【题目】向12.2克碳酸钠和硫酸钠的混合物加入一定质量的稀硫酸后恰好完全反应,测得反应前后烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图。其中烧杯的质量为30克(已知Na2CO3+H2SO4=Na2SO4+H2O+CO2↑)。试计算:
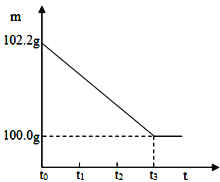
(1)生成气体的质量为 克。
(2)固体混合物中碳酸钠的质量是多少克?
(3)计算反应后溶液中溶质硫酸钠的质量分数(写出计算过程)
【答案】(1)2.2 (2) 20% (3)见解析
【解析】
试题分析:根据质量守恒定律知道生成气体的质量=102.2克-100.0克=2.2克
解:设固体混合物中Na2CO3的质量为x , 反应生成Na2SO4的质量为y,
Na2CO3+ H2SO4 = Na2SO4 + CO2↑+ H2O
106 142 44
x y 2.2
比例式为:106:X=142:Y=44:2.2克 解得:X=5.3g ,y=7.1g
反应后所得溶液质量= 100g-30g =70g
反应后所得溶液中溶质质量=(12.2g-5.3g)+7.1g =14g
则反应后溶液中溶质硫酸钠的质量分数=(14g ÷70g)×100% = 20%


科目:初中化学 来源: 题型:
【题目】在一烧杯中盛有22.3g Na2CO3和Na Cl组成的固体混合物,加足量水溶解,制成溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:
请根据题意回答问题:
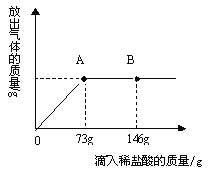
(1)当滴加了73g稀盐酸时,放出气体的总质量为 g。
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式) 。
(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题。

(1)写出图中仪器a的名称: 。
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为 ,可选择的发生装置为 (填字母)。
(3)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为 ,该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的 口(填“①”或“②”)通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于氧气的说法正确的是( )
A.氧气能支持燃烧,可作燃料
B.水生生物能依靠溶于水中的氧气而生存
C.氧气能跟所有物质发生氧化反应
D.氧气约占空气总体积的78%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于过滤的操作中,不正确的是
A、液体沿玻璃棒流进过滤器 B、漏斗里的液体液面应低于滤纸边缘
C、漏斗下端的管口紧靠烧杯的内壁 D、为加速过滤,用玻璃棒搅动漏斗里的液体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化钛(TiO2)是许多反应的催化剂。工业上用钛铁矿【主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2(不与H2SO4反应且不溶于水)】作原料,制取二氧化钛及绿矾(FeSO4·7H2O),其生产流程如下:
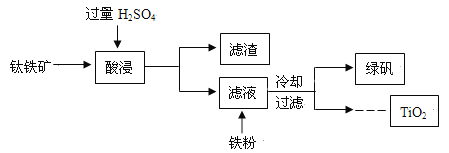
(1)加入H2SO4后,发生的反应有![]() 和 。
和 。
(2)加入铁粉,发生置换反应的化学方程式为 。
(3)以TiO2为原料还可以制取金属Ti。请将其中的一步反应的化学方程式补充完整:TiO2+2Cl2+C![]() TiCl4 + 。
TiCl4 + 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去下列物质或溶液中杂质(括号内为杂质)的方法,合理可行的是( )
A.氧化钙(碳酸钙) 加水、过滤
B.氯化亚铁(氯化铜) 加足量铁粉、过滤
C.硫酸(硫酸钠) 加入适量氯化钡试剂、过滤
D.盐酸钾(氢氧化钾) 通入足量二氧化碳气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用久置的镁条做实验时,需要用砂纸把表面的灰黑色打磨掉,直到露出光亮的银白色.实验小组同学对镁条表面“灰黑色外衣”的成分进行如下探究.
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【猜想与假设】Ⅰ.是镁与空气中的氧气反应生成的氧化镁.
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质.
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁.
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是 .
【查阅资料】
①碱式碳酸镁的性质有:受热可分解;常温下能与稀硫酸反应.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O.
同学们认为碳与浓硫酸反应生成三种产物的共同点是 .
【进行实验】(1)同学们用久置的镁粉进行了如下实验.
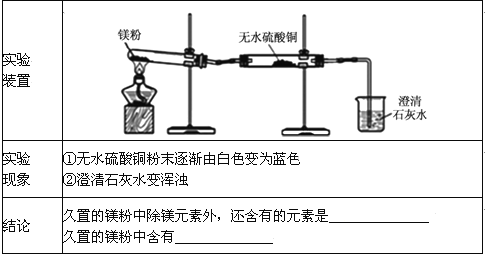
(2)同学们发现,经加热一段时间后,试管中镁粉会突然“噗”地燃烧起来,出现红热,很快停止,并有黑色固体粘附在试管壁上.于是将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失.请写出有气体生成的一个反应化学方程式 .
(3)将实验(2)试管中的混合物进行 (填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热.黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生.则黑色固体为________________.
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁.
【反思与评价】
有的同学提出,实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com