
| A. |  分离KNO3和NaCl | B. | 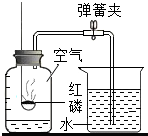 测定空气中O2含量 | ||
| C. | 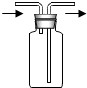 收集CO2气体 | D. |  用氢气还原氧化铜 |
分析 A、根据硝酸钾和氯化钠都易溶于水分析;
B、根据测定氧气含量的方法分析;
C、根据二氧化碳的密度比空气大分析;
D、根据氢气还原氧化铜的注意事项分析.
解答 解:A、硝酸钾和氯化钠都易溶于水,因此不能通过过滤进行分离,故不能达到实验目的;
B、红磷燃烧生成五氧化二磷,消耗了氧气,使瓶内气压减小,所以水会进入瓶内,根据进入水的体积测定出消耗的氧气的体积,故能达到实验目的;
C、二氧化碳的密度比空气大,所以气体要从长管进,短管出,故不能达到实验目的;
D、氢气还原氧化铜时,导管要伸到试管的底部,试管口要去掉橡皮塞,故不能达到实验目的;
故选项为:B.
点评 解答本题关键是要知道过滤操作的目的,知道氢气还原氧化铜的注意事项,知道空气中氧气含量的测定方法,知道二氧化碳的收集方法.


科目:初中化学 来源: 题型:选择题
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
| A. | 表中m的值为4.2 | |
| B. | 物质X由碳、氧元素组成 | |
| C. | 物质X由碳、氢元素组成 | |
| D. | 生产二氧化碳和水的分子个数比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
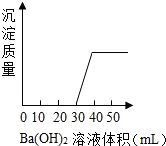 有一混合物是由盐酸、碳酸钠、硫酸、氯化铜、硝酸钾五种物质中的一种或几种混合而成.向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.据此回答:
有一混合物是由盐酸、碳酸钠、硫酸、氯化铜、硝酸钾五种物质中的一种或几种混合而成.向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.据此回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可以用铁桶盛放浓硫酸,但在清洗盛放过浓硫酸的铁桶时,不能遇明火 | |
| B. | 茶壶里的水垢,可以用醋酸或纯碱溶液除去 | |
| C. | 用天平称取NaOH固体时,必须将NaOH固体放在称量纸上 | |
| D. | 除去硫酸铁溶液中混有的硫酸,可以往其中加入铁粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质A中必然含有C、H、O三种元素 | |
| B. | 物质A中必然含有C、H元素,不含有O元素 | |
| C. | 物质A中必然含有C、H元素,可能含有O元素 | |
| D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com