草酸亚铁晶体(化学组成为FeC
2O
4?xH
2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

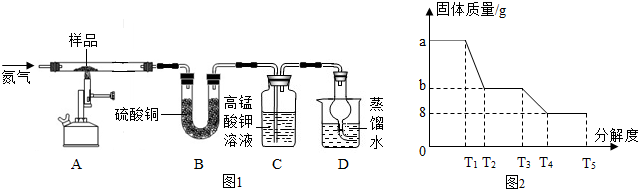
草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO
4足量):
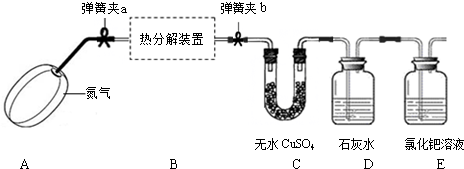
【实验步骤】:
①连接好装置,
检查气密性
检查气密性
;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④
关闭弹簧夹a
关闭弹簧夹a
,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
|
装置B的质量(/g) |
装置C的质量(/g) |
| 实验前 |
145.8 |
168.2 |
| 实验后 |
140.4 |
170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了
水
水
,FeC
2O
4?xH
2O中x的值为
2
2
;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了
CO
CO
;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了
CO2
CO2
;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(提示:相对分子质量分别为FeC
2O
4:144; H
2O:18)
FeO
FeO
;
(5)实验过程中,鼓入氮气的目的是
排尽装置中的空气,以免黑色的残留物(或FeO)被氧化
排尽装置中的空气,以免黑色的残留物(或FeO)被氧化
;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式
FeC
2O
4?2H
2O
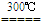
FeO+CO
2↑+CO↑+2H
2O
FeC
2O
4?2H
2O
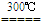
FeO+CO
2↑+CO↑+2H
2O
;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁.你认为这种说法是否正确?请说出可能的理由
不正确,因为温度达不到工业炼铁所需的高温,所以不能相互反应生成Fe
不正确,因为温度达不到工业炼铁所需的高温,所以不能相互反应生成Fe
;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?
没有尾气处理装置,会造成CO污染空气;
没有尾气处理装置,会造成CO污染空气;
;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式
4FeO+O2═2Fe2O3
4FeO+O2═2Fe2O3
.





 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O