
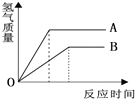
 等质量的A、B两种金属,分别与相同质量分数的足量稀盐酸反应(已知A、B在生成物中均为+2价),生成氢气的质量与反应时间的关系如右图所示,下列叙述正确的是( )
等质量的A、B两种金属,分别与相同质量分数的足量稀盐酸反应(已知A、B在生成物中均为+2价),生成氢气的质量与反应时间的关系如右图所示,下列叙述正确的是( )| A. | 产生氢气的速率是B>A | B. | 相对原子质量是B>A | ||
| C. | 生成氢气的质量是B>A | D. | 金属活动性顺序是B>A |
分析 根据等质量的A、B两种金属,活动性强的,与酸反应的速度就快,反应完用的时间就短.所以通过图表中的反应时间我们可判断A、B两种金属的活动性强弱.根据金属与酸反应产生氢气的质量公式:生成氢气的质量=$\frac{金属的化合价}{该金属的相对原子质量}$×金属质量,我们可以比较A、B两种金属相对原子质量的大小进行分析.
解答 解:A、根据反应时间,可知产生氢气的速度A>B,故A错误;
B、根据金属与酸反应产生氢气的质量公式:生成氢气的质量=$\frac{金属的化合价}{该金属的相对原子质量}$×金属质量,因为金属是等质量的,化合价又相等,所以氢气的质量越多,该金属的相等原子质量越小.故相对原子质量较大的是B,故B正确;
C、根据图表中纵坐标可知生成H2的质量A>B,故C错误;
D、根据图表中A反应时间短,可知A的活动性比B强,故D错误.
故选:B.
点评 本题考查了学生观察图表的能力,要求学生会根据图表判断金属的活动性,生成氢气质量的多少,反应速度的快慢,金属相对原子质量的大小.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 验证猜想 | 实验操作 | 实验现象 | 实验结论 |
猜想① | 燃烧更剧烈 | ||
猜想② | 燃烧更剧烈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
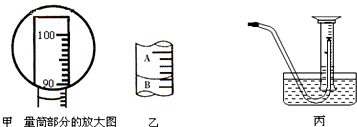
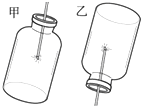 装满氧气的集气瓶,如图所示,当用带火星的木条分别以甲、乙两种方式迅速插入瓶中,木条复燃,而且在甲中燃烧比乙中更旺更持久.上述实验证明氧气具有的性质是氧气能支持燃烧;氧气的密度比空气的大.
装满氧气的集气瓶,如图所示,当用带火星的木条分别以甲、乙两种方式迅速插入瓶中,木条复燃,而且在甲中燃烧比乙中更旺更持久.上述实验证明氧气具有的性质是氧气能支持燃烧;氧气的密度比空气的大.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com