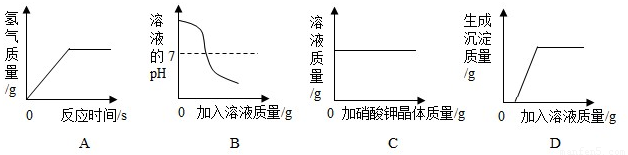
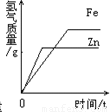
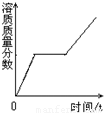
分析:解此题需知一定量的稀硫酸与锌粒反应,氢气的量逐渐增多,反应停止,氢气的量就不再改变;向稀盐酸中滴加过量的氢氧化钠溶液,PH是逐渐增大的;熟悉饱和溶液的概念,就可以知道t℃时,饱和硝酸钾溶液中加入硝酸钾晶体,不会继续溶解,溶液质量不变;向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液,发生的反应可以看做碳酸钠先和盐酸反应,此时没有沉淀产生,盐酸反应完后,碳酸钠才和氯化钙反应产生沉淀.
解答:解:A、锌加入稀硫酸中立刻反应产生氢气,稀硫酸反应完后,氢气的量就不再改变,故A对;
B、稀盐酸溶液呈酸性pH小于7,向其中加入过量的氢氧化钠(pH大于7)溶液,随着盐酸的消耗Ph逐渐增大直至恰好反应时pH=7,再滴加氢氧化钠则溶液的pH呈碱性pH会大于7,故B错;
C、t℃时,饱和硝酸钾溶液不能继续溶解硝酸钾晶体,所以硝酸钾溶液质量不变,故C对;
D、向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液,发生的反应可以看做碳酸钠先和盐酸反应,此时没有沉淀产生,盐酸反应完后,碳酸钠才和氯化钙反应产生碳酸钙沉淀,故生成沉淀的量是先为0,再不断上升直至完全反应沉淀的量不再增加,故D对;
故选B
点评:解此类图象题时首先应认真读懂题目中有限的文字信息,再次要对整个图象进行多角度的分析.



 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案