
����Ŀ��ij��ѧ��ȤС����ʵ������̽��ijЩ�ᡢ���֮���Ƿ������ֽⷴӦ��
��ʵ����̽������д�±����ա�
���� |
|
|
��Һ����_____ |
���� | �����ݲ��� | ������_____�� | ��Һ�ɺ�ɫǡ�ñ����ɫ |
ʵ�� ���� | ��ѧ����ʽ�� _____�� | ��ѧ����ʽ�� H2SO4+Ba(NO3)2=BaSO4��+2HNO3 |
ͼ����?�������������� _____�������ӷ��ţ��� |
���� | �����������������_____����ˮ����ʱ�����ֽⷴӦ���Է����� | ||
����չ��Ӧ�ã���ʵ��һ����������Ӧ����ϲ���Һ����ͬһ�ྻ���ձ��У����������룩����ʵ�鼰������ͼ��
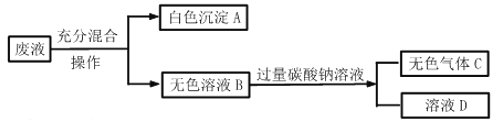
��1����ɫ��ҺB��pH_____7������<������>������=������
��2����ɫ����A��_____��
��3����ɫ��ҺB�г��˺��з�̪�⣬һ�������е�������_____��
���𰸡���̪��Һ ������ɫ���� H2SO4+Na2CO3=Na2SO4+CO2��+H2O SO42- ���� �� BaSO4 ����
��������
[ʵ����̽��]��д�±����ա�
���� |
|
|
��Һ������̪��Һ |
���� | �����ݲ��� | ������������ɫ������ | ��Һ�ɺ�ɫǡ�ñ����ɫ |
ʵ�� ���� | ��ѧ����ʽ�� H2SO4+Na2CO3= Na2SO4+CO2��+H2O�� | ��ѧ����ʽ�� H2SO4+Ba(NO3)2=BaSO4��+2HNO3 |
ͼ����?�������������� SO42-�������ӷ��ţ��� |
���� | �������������������������ˮ����ʱ�����ֽⷴӦ���Է����� | ||
[��չ��Ӧ��]
��1����ɫ��ҺB����̼���Ʒ�Ӧ��˵�������ᣬpH��7��
��2����������ʵ�����ܹ������ij���ֻ�����ᱵ�����BaSO4����
��3����ɫ��ҺB��һ�����з�Ӧ���������ᣬ�����������ᣬ������ᡣ��


 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ���Ȼ�þ����ͼ�ǴӺ�ˮ����ȡþ�ļ����̣�����ȡMg�Ĺ����У�
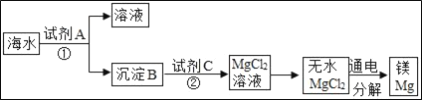
��1���Լ�A���ѡ��_____�����ҹ��зḻ��ʯ��ʯ��Դ���ǣ�������B���Լ�C���������кͷ�Ӧ�������B�Ļ�ѧʽΪ_____��
��2������ˮMgCl2��ȡMg�Ļ�ѧ����ʽΪ_____��
��3����ˮ�������Ǻ���MgCl2����Һ������ͨ�������������õ���MgCl2��Һ�кβ�ͬ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��θ���������ÿ���ҩ��������ᷴӦ������ͼΪij����ҩ˵���鲿�����ݣ���ȤС��Ը�ҩ�↑չ����̽�����ش��������⣺
I����ҩ������õ�̽����
��֪����̼��þ[��ѧʽΪAlMg��OH��3CO3]�����ᷴӦ�Ļ�ѧ����ʽΪ��![]()
��1������Ӧ����������ͨ�����ʯ��ˮ�����۲쵽��������_____����Ӧ�Ļ�ѧ����ʽΪ_____��
��2���������к���Al3+��Mg2+��OH����CO32������ϸ����������ᷴӦ�Ļ�ѧ����ʽ��������ҩ���������ã�����θҺ���ԣ�������_____��_____���������ţ���
II�����÷�����̽��
�ÿ���ҩΪʲôҪ�������á���С���������ǡ���ͬ������ҩƬ�������ã������ĸ����θ�ᡱ��С������Ϊ�������ҩ�ォ��θҺ�е����ᷴӦ�족��
��3����Ȼ��С������Ǵ���ģ�ԭ����_____��
��4��С�����������ʵ����֤���Լ��IJ��룺
[ʵ��1]��һƬ������ҩƬ�����Թ��У������м���5mL 5%��ϡ���
[ʵ��2]��һƬ������ҩƬ���������Թ��У������м���5mL 5%��ϡ���ᣮ
ʵ��ʱ��Ӧ�۲쵽������Ϊ_____��
III����Ҫ�ɷֺ�����̽��
��5����ȤС��ȡ3ƬҩƬ���������Թ��У��������������ϡ���ᣬ��ַ�Ӧ��ų�����0.44g����ͨ�����㣬ÿƬҩ���к���AlMg��OH��3CO3�������Ƕ��٣������������0.1��_____��
����֪��ҩ�����������ɷֲ���ϡ���ᷴӦ��AlMg��OH��3CO3����Է�������Ϊ162��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H��C��N��O��Na��S��K����Ԫ���У����ʵ���ѧ������գ�
(1)�����к�����ߵ�Ԫ��_____��(2)�����к����������嵥��______��(3)���ʯ_____��(4)�������ӵ�����_____��(5)�����н���Ԫ�صĻ��ϼ�_______��(6)�������Ϸʵ���_______��(7)�����ﶼ�ǵ��ʵķֽⷴӦ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ȷ��ӳ��Ӧ��ϵ����
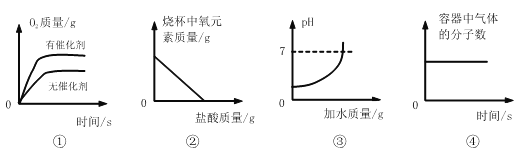
A. �ٵ���������Ũ�ȵĹ���������Һ������
B. ����ʢ��һ����̼��Ʒ�ĩ���ձ��м���ϡ����
C. ����һ�����������������в��ϼ�ˮ
D. ��һ��������̼����������������ܱ������г�ַ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪʵ�����г����������Ʊ����ռ�װ�á���ش��������⡣
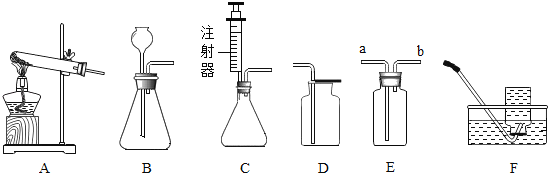
��1��ʵ�����ø��������ȡ���������Ӧѡ_____��_____������ĸ������Ӧ�Ļ�ѧ����ʽΪ_____��
��2��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ_____����ѡ��C������װ�ã�����Ϊѡ��C���ŵ���_____��
��3����ʹ��װ��E���ſ������ռ�������̼��������Ӧ��_____���a����b������ͨ�룻��ʹ��װ��E����ˮ���ռ�������������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
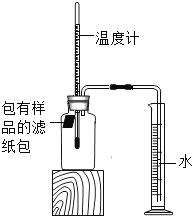
����Ŀ��С����������ʴ��������̽��������ʱ����������Ʒ����ֽ���ô�ͷ��̶��������ϣ�Ѹ��������װ����ͼ���۲쵽��Ͳ��ˮ�ص�������������ƿ�����ݻ�Ϊ146mL�������¶Ȼָ������£�����Ͳ��ˮ��߶Ȳ���ʱ��������ʱƿ��������������Ϊ�㣩����¼��ʼ��������Ͳ�Ķ����Լ�����ʱ�������
��� | ��Ʒ | ��Ͳ��ʼ ����/mL | ��Ͳ���� ����/mL | ����ʱ�� /min |
1 | 1g���ۡ�0.2g̼��10��ˮ | 100 | 70 | Լ120 |
2 | lg���ۡ�0.2g̼��10��ˮ������NaCl | 100 | 70 | Լ70 |
3 | ���� | 100 | 70 | Լ480 |
��1��ʵ��������˵��NaCl����_____����ʴ�����ʡ�
��2��ʵ�鿪ʼ���ƿ���¶�����������˵��������ʴ������_____������ȡ������ȡ������̡�
��3��ʵ�������ȡ����ֽ�����۲쵽�к���ɫ�������ɣ������ʵĻ�ѧʽ��_____��
��4����֪��̼�ܹ��ӿ����������ٶȣ�С����ͨ��ʵ����������̽��̼������ʴ���ʵ�Ӱ�죬���ڱ���հ״���дʵ��������Ʒ���_____��
��5����װ�û������ڲ��������������ĺ����������������ݼ������������������_____��С�������1λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���� X ����������ͭ��Ӧ��ȡͭ��ʵ��װ����ͼ��ʾ����ش��й����⡣

��1��ʵ�鿪ʼʱ����ͨһ��� X ���壬�ټ��ȵ�Ŀ����_____��
��2��ʵ�����һ��ʱ���A �������ڹ۲쵽�ĺ�ɫ������ɫ��B �����������������C �г���ʯ��ˮ����ǣ��� X ����Ϊ_____��д�� A �������ڷ�����Ӧ�Ļ�ѧ����ʽ_____��
��3����������������ͭ��Ӧ���� B ������пɹ۲쵽��������_____���ý���п����ϡ���ᷴӦ��ȡ��������ѡ���ʵ��װ�ã����ţ���������_____��
��4��ʵ������У�X ���������ͭ��Ӧ����������ͭ�������������м����������ͭ����ѧʽΪ Cu2O�������Ҫ�Է�Ӧ�� A �������������ɽ���̽���������������ܵ������_____�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ʒ�к��������Ȼ��ƣ���ȡ����Ʒ12g�ܽ���100gˮ�У�����������μ����Ȼ�����Һ�������ij���������Ȼ�����Һ��������ϵ��ͼ��ʾ��
���㣺
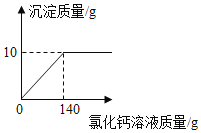
��1��������̼���Ƶ���������![]() �����ȷ��
�����ȷ��![]() ����ͬ
����ͬ![]() ______��
______��
��2��ǡ����ȫ��Ӧʱ��������Һ�����ʵ���������_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com