
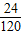 ,故该说法正确;
,故该说法正确;

科目:初中化学 来源: 题型:
 如图表示物质间发生化学变化的模型示意图,图中“
如图表示物质间发生化学变化的模型示意图,图中“ 、
、 ”分别表示两种不同元素的原子.下列说法正确的是( )
”分别表示两种不同元素的原子.下列说法正确的是( )| A、此反应有单质生成 | ||||
| B、该反应属于分解反应 | ||||
C、可表示2H2+O2
| ||||
D、可表示CO2+C
|
查看答案和解析>>
科目:初中化学 来源: 题型:
 北京时间3月11日13时46分,日本东北地区宫城县北部发生里氏9.0级强震.由于福岛第一核电站发生爆炸,导致放射性碘严重超标,我国部分城市市场发生顾客抢购加碘盐的情况.右图是超市销售的一种加碘盐标签上的部分文字说明.
北京时间3月11日13时46分,日本东北地区宫城县北部发生里氏9.0级强震.由于福岛第一核电站发生爆炸,导致放射性碘严重超标,我国部分城市市场发生顾客抢购加碘盐的情况.右图是超市销售的一种加碘盐标签上的部分文字说明.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com