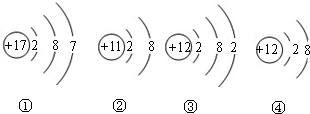解:问题一:海水富营养化,主要是因为陆地上排放的污水中含有较多的氮、磷元素,导致藻类疯长,故答案为:N、P;
问题二:海水中含量最多的金属是钠元素,钠是很活泼的,在自然界里以离子形式存在,海水中最多的物质是水,水是由水分子构成的,故答案为:Na
+、H
2O;
问题三:因氯化钠溶解度受温度影响不大,海水晒盐主要是蒸发水分,故选B;
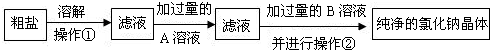
(1)主要利用泥砂不溶于水,采用过滤的方法除去,从氯化钠溶液中得到氯化钠晶体,应采用蒸发溶剂得到晶体,故答案为:
过滤;蒸发溶剂;
(2)除去氯化镁、氯化钙等杂质,实质是除去钙、镁离子,应用碱和碳酸盐将其转化为沉淀,并用酸将过量碱和碳酸盐反应掉,故答案为:a;d;
问题四:因晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH
4分子或1个游离H
2O分子.若晶体中每8个笼只有6个容纳了CH
4分子,另外2个笼被游离H
2O分子填充,则该化合物为可表示为6CH
4?48H
2O,即平均组成可表示CH
4?8H
2O,故选B;
根据H原子守恒可知,反应前有4+2n个H原子,则反应后水的系数为n+2,故答案为:n+2;
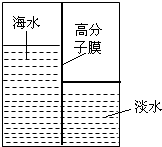
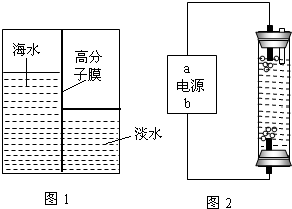
问题五:用高分子膜使海水淡化,类似于过滤,没有生成其他物质,所以海水淡化是物理变化,故答案为:物理;
问题六:由题意知反应物是氯化钠和水,生成物是氢氧化钠、氢气和氯气,反应条件是通电,因此根据化学方程式书写规则即可得化学方程式2NaCl+2H
2O

2NaOH+H
2↑+Cl
2↑;铁与稀硫酸反应生成硫酸亚铁和氢气,所以的化学方程式Fe+H
2SO
4=FeSO
4+H
2↑,这是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应.
故答案为:
2NaCl+2H
2O

2NaOH+H
2↑+Cl
2↑;Fe+H
2SO
4=FeSO
4+H
2↑;置换.
分析:本题应注意把课本所学知识和题中信息相结合,把握信息中的关键来灵活解答.
问题一:利用水体富营养化的原因来解答;
问题二:根据海水的成分和含量来解答;
问题三:根据氯化钠的溶解度分析海水晒盐的原理,利用不引入新的杂质,且将杂质离子转化为沉淀的方法来分析;
问题四:根据分子个数确定组成,利用原子守恒来配平化学方程式;
问题五:利用物质是否发生变化,是否有新物质生成来判断反应是物质变化还是化学变化;
问题六:根据反应物和生成物来书写化学方程式,要注意铁在溶液里发生置换反应时铁只能显示+2价.
点评:本题主要考查了水资源的污染和防治,并以此为核心综合了水的净化和化学方程式的书写,难度较大,涉及的内容多,要求学生具备牢固的基础.具有综合解决问题的能力.

 CO2+(n+2)H2O.
CO2+(n+2)H2O. 基本反应类型中的______反应.
基本反应类型中的______反应. 2NaOH+H2↑+Cl2↑;铁与稀硫酸反应生成硫酸亚铁和氢气,所以的化学方程式Fe+H2SO4=FeSO4+H2↑,这是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应.
2NaOH+H2↑+Cl2↑;铁与稀硫酸反应生成硫酸亚铁和氢气,所以的化学方程式Fe+H2SO4=FeSO4+H2↑,这是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应. 2NaOH+H2↑+Cl2↑;Fe+H2SO4=FeSO4+H2↑;置换.
2NaOH+H2↑+Cl2↑;Fe+H2SO4=FeSO4+H2↑;置换.

 6月5日是世界环境日,今年的主题是“海洋存亡,匹夫有责”,开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责.请回答下面关于海洋的几个问题:
6月5日是世界环境日,今年的主题是“海洋存亡,匹夫有责”,开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责.请回答下面关于海洋的几个问题: