
无土栽培是利用营养液栽培作物的一种方法(如图1)。
(1)下列化学肥料中属于复合肥的是 (填序号)。
①硝酸铵 ②碳酸氢铵 ③硝酸钾 ④硫酸钾
(2)小军要配制50g溶质质量分数为24%的硝酸钾溶液,需硝酸钾质量为 g。
(3)如图2A所示,称量时A出现了右盘低的现象,接下来的操作应该是 。
①左边的平衡螺母向左调至天平平衡 ②移动游码至天平平衡
③右盘中减少砝码至天平平衡 ④左盘中添加食盐至天平平衡
(4)量取水时,如果按照图2B的方法读数,会使配制的溶液溶质质量分数 (填“偏大”或“偏小”);图2C中用玻璃棒搅拌的作用是 。
(5)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图3所示的实验。
根据以上实验,请你进行有关推断。
①由实验1可确定原营养液中一定没有的物质是 ;
②根据实验1、实验2推测原营养液的组成可能有 种情况;
③若测得原营养液中K+和Cl一的数目之比为3:1,则原营养液的组成中的溶质是 。
(1)③(2)12 (3)④ (4)偏小;加快硝酸钾溶解速度
(5)①K2CO3 ②两 ③硝酸钙、氯化钾、硝酸钾[Ca(NO3)2、KCl、KNO3]
解析试题分析:(1)同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。①硝酸铵中只含有氮元素,不是复合肥;②碳酸氢铵中只含有氮元素,不是复合肥;③硝酸钾中含有氮元素和钾元素,属于复合肥;④硫酸钾中只含有钾元素,不属于复合肥.故选③。
(2)溶液质量与溶质质量分数的乘积是溶质的质量,则需用硝酸钾的质量为:50g×24%=12g。
(3)在称量中天平发生偏转时要么加药品,要么减药品,出现了右盘低的现象说明药品少了,应该增加食盐至天平平衡,故选④。
(4)熟记常见仪器的名称,仰视读数量取水时看到的读数偏小,但量取到的液体正好偏多,水多了,溶质质量分数就偏小;玻璃棒搅拌目的是加速氯化钠溶解。
(5)①实验1中把碳酸钠加入混合物的溶液中,产生了白色沉淀,根据所给的物质中能和碳酸钠产生沉淀的只有硝酸钙,同时也说明在混合物中没有碳酸钾。
②实验2中把硝酸银加入营养液中产生了白色沉淀,根据所给的物质中能和硝酸银产生沉淀的只有氯化钾,而两个实验中均没有提到硝酸钾,所以硝酸钾可能有,也可能没有,这样综合两个实验可以得出营养液中可能有的物质存在两种组合:一是硝酸钙、氯化钾,二是硝酸钙、氯化钾、硝酸钾。
③氯化钾中钾离子和氯离子的个数比为1:1,而溶液中钾离子和氯离子的个数比我3:1,所以我们根据溶液中的电荷守恒我们可以得出该营养液的组合中还含有硝酸根离子,即硝酸钾,故本题答案为:硝酸钙、氯化钾、硝酸钾[Ca(NO3)2、KCl、KNO3]。
考点:考查常见化肥的种类和作用;实验探究物质的组成成分以及含量;称量器-托盘天平;一定溶质质量分数的溶液的配制


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:填空题
从海水得到的粗盐,往往含有可溶性杂质(主要有Ca2+、Mg2+、SO42-)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。粗盐提纯的部分流程如下:其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠,除去滤液中的Ca2+
操作②:加入过量的X,除去滤液中的Mg2+
操作③:加入过量的氯化钡,除去滤液中的SO42-
请回答:(1)操作中的物质X为 ,正确的操作顺序为 (填序号),为最终获得精盐,操作①、②和③后还需增加的操作是 ;
(2)滤液二中加入适量稀盐酸的目的是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
无土栽培是利用营养液栽培作物的一种方法.
(1)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量
为 g.
(2)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.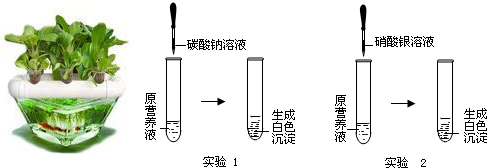
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是 。
②根据实验1、实验2推测原营养液的组成可能有 种情况;
③若测得原营养液中K+和Cl一的数目之比为1:1,则原营养液的组成中的溶质是
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
海洋为我们提供了丰富的资源,二十一世纪是海洋开发与利用的世纪,请围绕“海洋”这个话题回答以下问题:
(1)下图1是我们从海水中提取镁的流程图: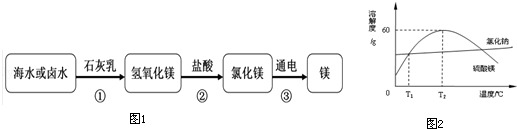
①上述一系列转化过程中,属于中和反应的是 (用化学方程式表示)
②海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳.
乙:高温加热蒸发海水后,加入石灰乳.
丙:向晒盐后的卤水中,加入石灰乳.
通过分析比较,你认为 的设想最为经济合理(选填“甲”、“乙”或“丙”).
(2)关于海水“制碱”中得到的“碱”的成分,甲同学认为是氢氧化钠,乙同学认为是碳酸钠,为确定其成分,甲、乙同学各做了以下两个实验:
①甲向“碱”溶液中加入酚酞,观察到酚酞变红,于是认为“碱”是氢氧化钠.
②乙向“碱”溶液中加入氢氧化钙溶液,产生白色沉淀,于是认为“碱”是碳酸钠.
你同意 (填甲或乙)同学的观点,请指出另一个同学实验设计的不合理之处
(3)从海水晒盐留下的“苦卤”中加工得到不纯的硫酸镁晶体,其中含有少量氯化钠,根据溶解度曲线图2回答下列问题:
①t1℃时,等质量的水中最多溶解的硫酸镁质量 (填大于、小于或等于)最多溶解的氯化钠的质量.
②t2℃时,向50克水中加入50克硫酸镁,所得溶液的溶质质量分数是 .
③要除去少量的氯化钠,得到较纯净的硫酸镁,可采用的方法是 .
A.过滤
B.蒸干水分
C.将t2℃硫酸镁的饱和溶液升温,析出晶体后过滤.
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
氢氧化钠是化学实验室中常用的试剂.
(1)氢氧化钠固体曝露在空气中,容易吸收水分而使表面覆盖一层溶液(这一现象又叫“潮解”);它还能 ,这一变化的化学方程式可表示为 .所以氢氧化钠固体必须密封保存.
(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,反应的化学方程式为:SiO2+2NaOH═X+H2O,试推断X的化学式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
通过一年的化学学习,我们认识了“酸”和“碱”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的 离子(填符号),因此,它们有很多相似的化学性质,如: 等(写二条即可).
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,如:干燥 等气体,氢氧化钙可由生石灰与水反应制得,化学方程式为: .
(3)酸和碱能发生中和反应,它在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等杂质,可用熟石灰进行处理,反应的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
在①浓硫酸、②氢氧化钠、③稀盐酸、④氢氧化钙这四种物质中选择适当物质的序号填空:
(1)常用于干燥二氧化碳气体的干燥剂是 .
(2)实验室制取二氧化碳气体的酸是 .
(3)实验室用于检验二氧化碳气体的碱是 .
(4)俗名为烧碱的物质是 .
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
如表是市场上销售的一种常见氮肥的包装说明书。请阅读有关内容后,回答下列问题:
| 主要成分 | NH4Cl |
| 保存方法 | 干燥阴凉处存放 |
| 含氮量 | ≥25% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如下:
请回答下列问题:
(1)A的化学式是 。
(2)写出步骤③发生反应的化学方程式 。
(3)在工业上,熟石灰可用于生产烧碱。在农业上,它的一种用途是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com