
科目:初中化学 来源:江苏省盐城市阜宁县2019届九年级下学期第二次学情调研化学试卷 题型:单选题
以下除去杂质(括号中为杂质)操作方法最为恰当的是
A. Zn 粉(ZnO):加入足量稀硫酸充分反应后过滤
B. CaCO3(Na2CO3):加足量水溶解,过滤,滤液蒸发结晶
C. CO2(CO):通入氧气点燃
D. Zn(NO3)2溶液(AgNO3):加入过量Zn粉充分反应后过滤
查看答案和解析>>
科目:初中化学 来源:江苏省江阴市澄要片区2019届九年级下学期5月中考模拟化学试卷 题型:单选题
利用下列实验装置进行实验,能达到目的的是
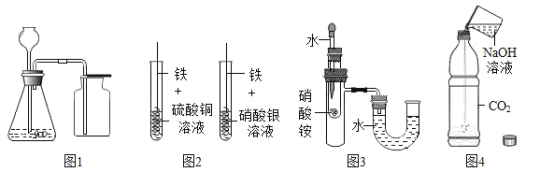
A. 图1装置可用锌粒和稀硫酸制取H2或用大理石和稀盐酸制取CO2
B. 图2装置铁丝表面均有固体析出可探究金属活动性:Fe>Cu>Ag
C. 图3装置看到U型管水面左高右低可验证NH4NO3溶于水吸热
D. 图4装置根据软塑料瓶变瘪可证明CO2能与NaOH反应
查看答案和解析>>
科目:初中化学 来源:江苏省南京市溧水区2019届九年级下学期中考一模化学试卷 题型:单选题
在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前、反应中及反应结束前某时刻的各物质的质量(如表)。表中x、y、m、n分别表示相应物质的质量。下列数据正确的是( )
甲 | 乙 | 丙 | 丁 | |
反应前质量/g | 70 | 14 | 6 | 10 |
反应中质量/g | x | 11 | m | n |
反应结束前质量/g | 42 | y | 40 | 10 |
A. x=56 B. y=6 C. m=17 D. n=8
查看答案和解析>>
科目:初中化学 来源:江苏省南京市溧水区2019届九年级下学期中考一模化学试卷 题型:单选题
下列物质中,计入“空气污染指数”的是( )
A. 氧气 B. 氮气 C. 二氧化碳 D. 可吸入颗粒物
查看答案和解析>>
科目:初中化学 来源:安徽省滁州市凤阳县2019届九年级下学期中考一模化学试卷 题型:科学探究题
重庆一中化学兴趣小组的同学将氢氧化钠溶液和稀硫酸混合,没有观察到明显的现象,他们对此提出了如下问题并进行了相应探究:
问题一:二者之间是否发生了反应?他们设计了如下方案证明二者之间确实发生了反应:
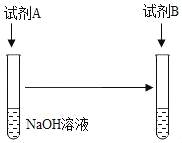
(1)可以选择的试剂组合有_____(填序号)。
①试剂 A:足量稀硫酸,试剂 B:MgCl2溶液
②试剂 A:足量稀硫酸,试剂 B:铁粉
③试剂 A:少量稀硫酸,试剂 B:MgCl2溶液
④试剂 A:少量稀硫酸,试剂 B:铁粉
(2)小兰认为,若选用_____溶液,不管加入顺序如何,只需控制加入稀硫酸的量也 能证明二者发生了反应。
问题二:反应后溶液中溶质有哪些?
(猜想假设)猜想一:只有 Na2SO4;猜想二:Na2SO4 和_____;猜想三:Na2SO4 和 H2SO4。
(查阅资料)①Na2SO4 溶液显中性,②Na2SO4+BaCl2=BaSO4↓+2NaCl。
(实验操作)分别取少量反应后的溶液于试管中,进行如下实验:
实验编号 | 实验过程 | 实验现象 |
① | 加入酚酞溶液 | 不变红 |
② | 加入少量 BaCl2溶液 | 产生白色沉淀 |
③ | 加入少量 Na2CO3溶液 | _____(填“有”或“无”)气泡产生 |
(实验结论)猜想一成立。
(实验反思)小娜认为,实验_____(填实验编号)可省略。 小秋用精密仪器检测反应后溶液中离子的个数比,也得出了相同结论,则测得溶液中的 Na+和 SO42﹣个数比为_____。
查看答案和解析>>
科目:初中化学 来源:安徽省滁州市凤阳县2019届九年级下学期中考一模化学试卷 题型:单选题
人体生长发育都离不开钙,日常食用的食物要适当补钙。如图是它在元素周期表中的信息。下列有关说法错误的是( )
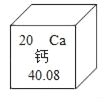
A. 元素名称为钙 B. 元素符号为Ca
C. 原子序数为20 D. 相对原子质量为40.08g
查看答案和解析>>
科目:初中化学 来源:天津市滨海新区2019届九年级下学期第二次模拟考试化学试卷 题型:填空题
日常生活与化学有着密切的联系,现有①活性炭 ②乙醇 ③氯化钠 ④氢氧化铝 ⑤氧气 ⑥氮气,请按要求填空(填序号):
(1)在生活中可作为调味剂和防腐剂的是_____;
(2)可用来去除色素或冰箱异味的是_____;
(3)可作为制备硝酸和氮肥的主要原料_____;
(4)可通过粮食发酵制备作为燃料的是_____;
(5)可用来治疗胃酸过多的是_____;
(6)植物光合作用生成的气体是_____。
查看答案和解析>>
科目:初中化学 来源:江苏省南京市高淳区2019届九年级下学期中考二模化学试卷 题型:科学探究题
某实验小组同学对铁粉和氧化铜的混合物与足量的稀硫酸混合后,体系中各反应的先后顺序进行研究。
氧化铜与稀硫酸反应的化学方程式为________________。
(进行实验)以下实验中所用硫酸都是过量的。
实验1:将铁粉和氧化铜的混合物与60mL、10%稀硫酸混合,实验记录如下。
序号 | 铁粉/g | 氧化铜/g | 实验现象 |
1-1 | 0.56 | 1.6 | 立即出现红色固体,无气泡产生,充分反应后溶液呈蓝色 |
1-2 | 1.12 | 1.6 | 立即出现红色固体,无气泡产生,充分反应后溶液呈浅绿色 |
1-3 | 1.68 | 1.6 | 立即出现红色固体,待红色固体不再增加后产生大量气泡,充分反应后溶液呈浅绿色 |
实验2:将1.12g铁粉和1.6g氧化铜的混合物与30mL不同浓度的硫酸混合,实验记录如下。
序号 | 硫酸浓度/% | 实验现象 |
2-1 | 20 | 立即出现红色固体,无气泡产生,充分反应后溶液呈浅绿色 |
2-2 | 30 | 立即出现红色固体,瞬间产生大量气泡,充分反应后溶液呈浅蓝色 |
2-3 | 50 | 立即出现红色固体,瞬间产生大量气泡,反应过程中生成红色固体的同时持续产生细小气泡,充分反应后溶液呈浅蓝色 |
(解释与结论)
(1)浅绿色溶液中一定含有的溶质是H2SO4、____。
(2)实验中出现红色固体反应的化学方程式为_________;
(3)依据实验1推测,在稀硫酸浓度为10%,且硫酸足量的条件下,铁粉、氧化铜与稀硫酸反应的先后顺序为________。
(4)对比分析实验1-2与1-3,解释实验1-2没有产生气泡的原因______。
(5)在实验1-3中,产生氢气的质量最多为____ g。
(6)根据实验2判断,下列说法不正确的是____(填字母序号)。
A 硫酸浓度为20%,CuO先于Fe与硫酸反应
B 硫酸浓度为40%,Fe将先于CuO与硫酸反应
C 硫酸浓度为50%,Fe与CuSO4反应的同时也与硫酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com