
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
 纸火锅(见图)在某地区悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;不会被火点燃.纸火锅烧不着的原因是纸火锅里的汤汽化时吸热,使温度达不到纸的着火点.
纸火锅(见图)在某地区悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;不会被火点燃.纸火锅烧不着的原因是纸火锅里的汤汽化时吸热,使温度达不到纸的着火点.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 该物质中碳元素的质量分数为40% | |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| C. | 该物质由碳、氢、氧元素组成 | |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
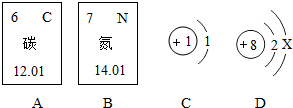 下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题:
下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com