
【题目】根据题目信息:用数字和化学符号填空。
【答案】![]()
【解析】
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行解答;
根据元素的正化合价数等于其原子的最外层电子数;进行解答;
根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,进行解答.
解答:解:
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个铝离子表示为:2Al3+;根据元素的正化合价数等于其原子的最外层电子数;由原子结构示意图可知,铝元素的化合价为+3;
根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,氧元素的化合价为-2,铝元素的化合价为+3,所以铝的氧化物的化学式为:Al2O3 ;
故答案为:2Al3+;+3;Al2O3 .


科目:初中化学 来源: 题型:
【题目】下图是一些常见物质的转化关系,其中C是无色无刺激性的气体,且能使澄清石灰水变浑浊;E是一种无污染的清洁能源,其燃烧产物是H。
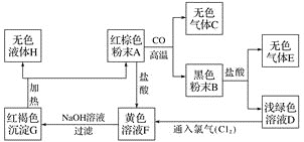
请根据上图,回答下列有关问题:
(1)红棕色粉末A和气体C、E的化学式分别为A________、C________、E:________。
(2)G转化为H和A的反应类型是________反应;B转化成E和D的反应类型是________反应。
(3)①A与盐酸反应的化学方程式为_______________________;
②D和氯气化合生成F的化学方程式为____________________________。
(4)以上图中无色气体C为中心,延展如图:
![]()
①请写出实现这两个转化的另一反应物J、K的化学式:J________、K________。
②请完善由CO和CaCO3分别转变成无色气体C的转化关系图,在箭号上注明必要的反应条件和其它反应物。
![]() _______________________
_______________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图回答简题
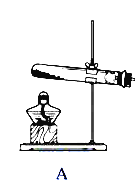

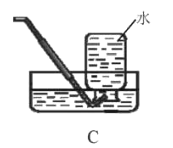
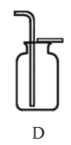
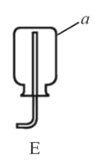
(1)写出仪器a的名称:_____。
(2)实验室用加热高锰酸钾的方法制取并收集氧气,应选用的装置为_____(填序号),该反应的化学方程式为_____。
(3)实验室用石灰石和稀盐酸反应制取并收集二氧化碳,应选用的装置为_____(填序号),该反应的化学方程式为_____。
(4)实验室制取气体时,连接好仪器装置,在装入药品前要检查装置的_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室污染成为环境保护的关注点。某学校排放的废水中含有碳酸钠,未经处理,会造成污染,化学兴趣小组的同学对废水处理设计了如图所示的实验方案。

试计算:
(1)反应生成CO2气体的质量是多少g。
(2)反应后所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包固体粉末,可能由CaCO3、CaO、Fe2O3 、KNO3、Na2CO3中的一种或几种组成。
为确定其组成,进行了如下图所示的实验(假设实验过程无损耗)。请回答:
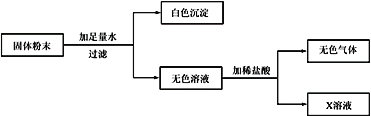
(1)白色沉淀是____;原固体粉末中一定含有___,该白色固体的可能组成有___种。
(2)氧化钙和水反应的化学方程式是____。
(3)若实验取固体粉末20.0g,生成白色沉淀10.0g,最后得到溶质质量分数为5.85%的X溶液200.0g(只含一种溶质),则原固体粉末由___组成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案的设计、实施和评价.
①方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃).测定某NaOH溶液的pH,pH_____7(选填“大于”、“等于”或“小于”).将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH 小于7.结论:稀H2SO4与NaOH溶液发生了化学反应,并且_____过量.
②方案二:根据图示实验步骤,观察到_____现象.

结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为_____.
③为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是_____(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度_____次.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)我市东部山区盛产石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析:
方案一: 取10g石灰石粉末样品置于下图所示装置,充分加热至质量恒定,冷却后称得固体质量为8.12g
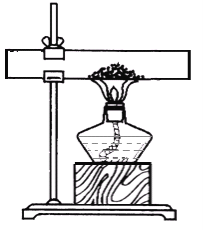
方案二:另取10g同质地石灰石颗粒样品,置于烧杯中加足量稀盐酸,充分反应后称得混合物的总质量减少了4.27g
相关资料:
当地石灰石含有的主要杂技为二氧化硅,其化学性质稳定,加热不易分解且不与盐酸发生化学反应.
计算出两种方案测得的石灰石中碳酸钙的质量分数:
(1)方案一中碳酸钙的质量分数是 ;
(2)方案二中碳酸钙的质量分数是 .(精确到0.1%)
比较两方案测量的结果,分析两方案误差较大的可能原因?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤燃烧后的煤灰粉末(主要含氧化铝、二氧化硅等物质)可制备碱式硫酸铝[Al2(OH)6-2X(SO4)X]溶液,并进行烟气脱硫的探究,其实验流程如下图所示:
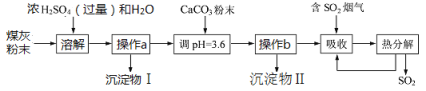
资料:二氧化硅难溶于水和酸,也不与其发生反应。H2SO3受热易分解,其酸性弱于H2SO4;H2SO4受热不易分解。
(I)Al2(OH)6-2X(SO4)X中铝元素的化合价为________。
(2)“溶解”时,先将煤灰粉末倒入烧杯中,接下来的具体操作是:___________,主要的反应方程式为_____________。
(3)操作a、b的名称为________,沉淀物Ⅰ的主要成分为_______________(填化学式)。
(4)不断加入CaCO3粉末使溶液的pH升高到3.6,其作用是____________________并使Al2(SO4)3转化为Al2(OH)6-2X(SO4)X。
(5)流程中,“热分解"时溶液中的部分H2SO3会被氧化为H2SO4,则完全“热分解”放出的SO2量总是__(填“大于”、“小于"或“等于”吸收的SO2量,“热分解"后循环利用的溶液pH_______(填“大于”、“小于"或“等于")吸收SO2之前的溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO3溶液,经过滤、洗涤、干燥、称量,得到143.5gAgCl固体;②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别 | 一 | 二 | 三 | 四 | 五 |
混合溶液质量/g | 200 | 200 | 200 | 200 | 200 |
铁屑质量/g | 6 | 9 | 12 | 15 | 18 |
析出铜的质量/g | 6.4 | 9.6 | m | 16 | 16 |
请分析计算:
(1)表中第三组实验的m值为_______。
(2)第_____组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少___________?(计算结果精确到0.1%)
(4)原混合溶液中FeCl2的质量分数为多少______________?(计算结果精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com