
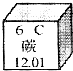
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.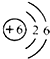 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01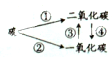
| ||
| ||
| ||
| ||
| 100 |
| X |
| 44 |
| 4.4g |
| 2.5g |
| 10g |
| ||
| ||
| ||
| ||


科目:初中化学 来源: 题型:
| 选项 | 物质 | 操作方法 |
| A | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
| B | NaNO3(Na2SO4) | 加入过量的Ba(NO3)2溶液,充分反应后过滤 |
| C | NaOH溶液(Na2CO3溶液) | 加入适量的CaCl2溶液,充分反应后过滤 |
| D | CuSO4溶液(硫酸) | 加入过量Cu0粉末,加热,充分反应后过滤 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目:初中化学 来源: 题型:
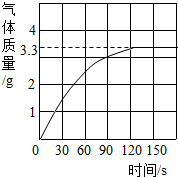 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.提示:反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑ Mg(OH)2+2HCl═MgCl2+2H2O
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.提示:反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑ Mg(OH)2+2HCl═MgCl2+2H2O查看答案和解析>>
科目:初中化学 来源: 题型:
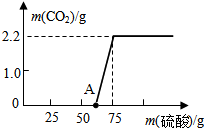 某校研究性学习小组进行了一个有趣的实验探究:
某校研究性学习小组进行了一个有趣的实验探究:查看答案和解析>>
科目:初中化学 来源: 题型:
| 水质主要成分(mg/L) | |
| 偏硅酸(H2SiO3) 28.9-42.9 碳酸氢根(HCO-3)173-205 氯离子(Cl-) 1.0-8.0 硫酸根 16.06-19.52 镁(Mg2+) 2.5-7.5 |
锶(Sr) 0.01-0.32 钙 5-45 钠(Na+) 45-70 钾(K+) 0.5-2.0 PH 7.8±0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com