按要求写出除去下列固体或溶液中所含杂质(括号内为杂质)的化学方程式:
ZnCl2(HCl);NaCl(CuCl2);CuO(Cu);CaO(CaC03).
(1)化合反应 ;
(2)分解反应 ;
(3)置换反应 ;
(4)复分解反应 .
【答案】
分析:化学方法除杂质一般是通过化学反应将杂质直接出去或将杂质转化为要保留的物质.书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据质量守恒定律的两个原则.本题中书写化学方程式时,还要符合基本反应类型的要求.
解答:解:(1)氧化铜中的杂质铜可以通过加热的方法使铜与空气中的氧气在加热条件下反应转化成氧化铜.
该反应由两种物质反应生成一种物质,符合化合反应的概念.
该反应的化学方程式为:2Cu+0
2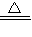
2CuO.
(2)氧化钙中的杂质碳酸钙可以通过高温的方法使碳酸钙在高温条件下分解转化成氧化钙.
该反应由一种物质反应生成两种物质,符合分解反应的概念.
该反应的化学方程式为:CaC0
3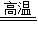
CaO+C0
2↑.
(3)氯化锌溶液中的杂质稀盐酸可以通过锌与稀盐酸反应的方法使稀盐酸转化成氯化锌.
该反应由一种单质和一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念.
该反应的化学方程式为:Zn+2HCl=ZnCl
2+H
2↑.
(4)氯化钠中的杂质氯化铜可以通过氯化铜与氢氧化钠反应的方法使氯化铜转化成氯化钠.
该反应由两种化合物相互交换成分形成两种新的化合物,符合复分解反应的概念.
该反应的化学方程式为:CuCl
2+2NaOH=Cu(OH)
2↓+2NaCl.
故答案为:
(1)2Cu+0
2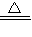
2CuO
(2)CaC0
3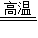
CaO+C0
2↑
(3)Zn+2HCl=ZnCl
2+H
2↑
(4)CuCl
2+2NaOH=Cu(OH)
2↓+2NaCl
点评:本题主要考查除杂的原理和方法、基本反应类型的应用、物质的简单分类和化学方程式的书写,难度较大.本题化学方程式的书写除了依据质量守恒定律和化学方程式的书写方法外,还要符合基本反应类型的概念和特点,符合用化学方法除杂质的原理,还要书写物质的简单分类,这些内容都是书写化学方程式时必须要考虑的问题.

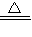 2CuO.
2CuO.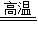 CaO+C02↑.
CaO+C02↑.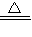 2CuO
2CuO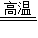 CaO+C02↑
CaO+C02↑

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案