
| A. | 过滤时,为加快过滤的速度,可用玻璃搅动漏斗里的液体 | |
| B. | 为了节约药品,可将实验用剩的药品倒回原试剂瓶中 | |
| C. | 给试管里的液体加热时,液体量可占试管容积的$\frac{1}{3}$-$\frac{2}{3}$ | |
| D. | 称量时,用镊子取放砝码 |
科目:初中化学 来源: 题型:选择题
| A. | 根据质量守恒定律可知X的化学式为H2SO4 | |
| B. | 该反应生成的CrO3与H2O的质量比为100:9 | |
| C. | 该反应过程中无需加热 | |
| D. | 该反应中的产物均为氯化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛分子是由一个碳原子和一个水分子构成的 | |
| B. | 甲醛分子中C、H、O的元素个数之比为l:2:1 | |
| C. | 甲醛中C、H、O的质量之比均为12:1:16 | |
| D. | 不同质量分数的甲醛水溶液中H、O的质量之比均为1:8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
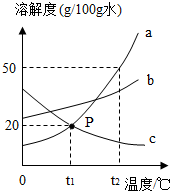 如图是a、b、c三种物质的溶解度曲线,下列分析正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析正确的是( )| A. | t1℃时,100g a物质饱和溶液中含有20g a物质 | |
| B. | t1℃时a、c两种物质的饱和溶液中溶质相等 | |
| C. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a>c | |
| D. | a物质中含有少量的b物质,可采用冷却热饱和溶液的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com