
在烧杯里加入6g质量的石灰石和44g质量的稀盐酸,完全反应后烧杯里剩余物质的质量为47.8g,(反应化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2)
(1)根据 定律,生成CO2气体的质量 ;
(2)参加反应的碳酸钙的质量是多少?
科目:初中化学 来源: 题型:计算题
科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。图甲是实验室制取并检验CO2的装置,图乙是对图甲实验装置的“微型”化改进后的装置。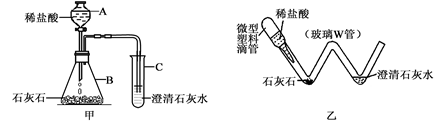
(1)图乙中微型塑料滴管在实验中的作用与图甲中的 仪器相同(填仪器名称)。
(2)通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,“微型”实验装置具有的优点是 。
(3)用乙装置完成“制取并检验CO2”的实验,消耗了1.46g10%的盐酸。请计算实验过程中产生CO2的质量是多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
市场上有一种外观类似黄金的Cu—Zn合金 ,现取合金粉末20g放入烧杯中,加入50 g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为69.8 g。 求:
①产生氢气的质量;
②求出该合金中铜的质量分数;
③稀硫酸中溶质的质量分数;
④反应后所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
小宇同学在实验室里将16 g高锰酸钾放在试管里加热制取氧气,反应一段时间后,他称得剩余固体物质的质量为14.4 g,试求:
①生成氧气为多少克?这些氧气在标准状况下的体积是多少升? (设标准状况下O2的密度为1.4 g/L)
②剩余固体物质中含有哪些物质,各有多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是34.4g,将杯内剩余物质过滤、洗涤、干燥后得滤渣2g。计算:
(1)生成氧气的质量。
(2)瓶内过氧化氢溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
28g石灰石样品与210.8g稀盐酸恰好完全反应后(样品中的杂质既难溶于水,又不与稀盐酸反应),生成了8.8g二氧化碳。(溶解在水中的二氧化碳忽略不计)计算:
(1)该石灰石样品中碳酸钙的质量分数。
(2)所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下: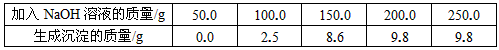
(1)得到沉淀的总质量为 g,该混合溶液中硫酸铜的质量为 g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某锌样品15g加入50g稀硫酸中(杂质既不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为64.6g。试计算:
(1)生成氢气的体积。(精确到0.1L,在标准状况下氢气的密度为0.9g/L)
(2)锌粒中所含锌的质量分数(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
盐碱湖中捞出来的纯碱中含有一定量的食盐,为测定其中碳酸钠的含量,化学小组的同学将某纯碱样品24.6g放入烧杯中,逐滴加入150g稀盐酸,恰好完全反应,待不再产生气泡时,得到168g的食盐溶液.计算原混合物中碳酸钠的质量分数和反应后溶液的溶质质量分数(CO2的溶解忽略不计).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com