
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
分析 向硫酸和硫酸铜的混合溶液滴加氢氧化钠溶液,硫酸、硫酸铜都可与氢氧化钠发生反应,由于硫酸的存在氢氧化钠与硫酸铜不能生成氢氧化铜沉淀,待硫酸反应完才能产生氢氧化铜沉淀;所以记录数据中,加入50.0g氢氧化钠溶液时产生沉淀的质量为0;而在加入氢氧化钠溶液200.0g以后沉淀质量不再变化,说明硫酸铜也已完全反应,故生成沉淀量最大值为9.8g;
根据硫酸铜与氢氧化钠反应的化学方程式,由沉淀氢氧化铜的质量可计算混合溶液中硫酸铜的质量及与硫酸铜发生反应的氢氧化钠的质量.
解答 解:(1)由记录数据表可知,至硫酸铜完全反应共生成蓝色沉淀9.8g;Cu(OH)2----CuSO4
根据化学变化前后元素质量不变,混合溶液中硫酸铜的质量=$\frac{9.8g×\frac{64}{98}×100%}{\frac{64}{160}×100%}$=16.0g;
故答案为:9.8;16.0;
(2)设与硫酸反应的氢氧化钠的质量为x,与硫酸铜反应的氢氧化钠的质量为y
H2SO4+2NaOH═Na2SO4+2H2O
98 80
9.8g x
$\frac{98}{80}=\frac{9.8g}{x}$
x=8.0g
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
80 98
y 9.8g
$\frac{80}{98}=\frac{y}{9.8g}$
y=8g
故参加反应的氢氧化钠溶液的质量=$\frac{8g+8g}{10%}$=160g
答:参加反应的NaOH溶液的总质量是160g
点评 学生应熟悉利用化学方程式计算的思路和格式,能利用恰好反应及元素守恒和分析数据来解答.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:初中化学 来源: 题型:解答题
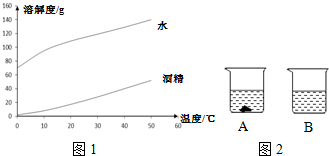
| 甲 | 乙 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 溶液在生命活动和生产、生活中都起到十分重要的作用.
溶液在生命活动和生产、生活中都起到十分重要的作用.| 实验编号 | a | b | c | d | e |
| 加入KNO3固体的质量 | 40 | 45 | 50 | 55 | 60 |
| 所得溶液质量 | 90 | 95 | 100 | 105 | 105 |
| 温度/ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 0.18 | 0.16 | 0.14 | 0.11 | 0.09 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.
硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com