解:(1)一氧化碳具有还原性,可将氧化铜火焰为铜,故可看到乙装置中黑色粉末变红;
(2)一氧化碳还原氧化铜生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
(3)一氧化碳有毒,要进行尾气处理,防止污染大气,图示装置没有;
(4)氢氧化钠溶液与二氧化碳反应生成碳酸钠,要证明原气体中含二氧化碳,甲装置中氢氧化钠溶液部分变质,可加入氯化钙溶液观察有沉淀生成,说明氢氧化钠变质;碳酸钠和氯化钙反应生成碳酸钙和氯化钠,方程式是:CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl;氯化钠和氯化钙溶液显中性,所以可静置,取上层清液于另一试管中,滴加酚酞溶液,若溶液变红,说明溶液中含有氢氧化钠;
若甲装置中氢氧化钠溶液完全变质,则加入氯化钙溶液有白色沉淀生成,滴加酚酞无变化;
(5)要除去甲装置中的杂质,使它变回纯净的氢氧化钠溶液,可加入适量的氢氧化钙溶液,碳酸钠和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,过滤即可;
故答案为:(1)黑色粉末变红; (2)澄清溶液变浑浊; (3)没有尾气处理装置;
(4)
| 实验步骤 | 实验现象 | 化学方程式 |
| (二) | ①氯化钙 | ②变红 | ①CaCl2+Na2CO3═CaCO3↓+2NaCl |
| (三) | | ②不变色 | |
(5)氢氧化钙溶液.
分析:(1)据一氧化碳具有还原性分析解答;
(2)一氧化碳还原氧化铜生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
(3)一氧化碳有毒,要进行尾气处理,防止污染大气;
(4)根据实验目的、物质的性质选择药品,碳酸钠可与氯化钙反应生成碳酸钙沉淀,氢氧化钠溶液显碱性,可使酚酞试液变红;
(5)据碳酸钠的性质及除杂原理分析回答.
点评:掌握氢氧化钠与二氧化碳的反应原理,一氧化碳的还原性,除杂原理等知识,并会灵活应用,能较好培养学生分析、解决问题的能力.

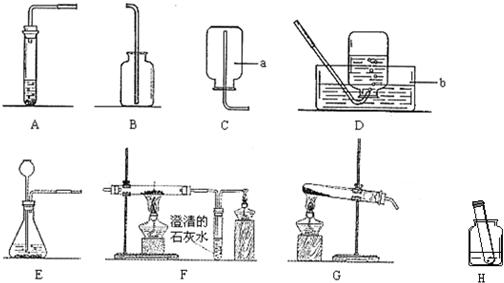
 如图是利用一氧化碳气体(可能含有二氧化碳)还原氧化铜的实验示意图.
如图是利用一氧化碳气体(可能含有二氧化碳)还原氧化铜的实验示意图.

 阅读快车系列答案
阅读快车系列答案
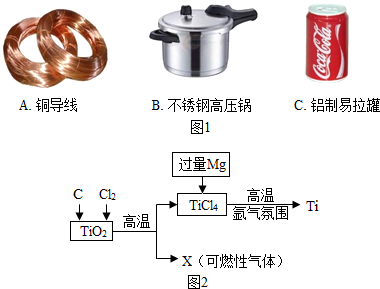 (2013?玄武区二模)金属在生产和生活中有广泛的应用.
(2013?玄武区二模)金属在生产和生活中有广泛的应用. (2012?天桥区二模)利用工业煤制乙二醇(C2H6O2重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题.
(2012?天桥区二模)利用工业煤制乙二醇(C2H6O2重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示.回答下列问题. (1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为
(1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为