



 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:

| 执行标准:GH1413-00 每瓶50片,净重40g 主要成分:碳酸钙 含钙量:每片含钙0.75g (中外合资xx公司出品)①通过计算说明此标签中的含钙量是否合理? ②如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片.请计算每天他需补充碳酸钙多少克? 查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 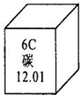 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容. 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.(1)右图为元素周期表中的一格,下列说法不正确的是 D D (填标号).A.碳元素属于非金属元素 B.碳原子核内质子数为6 C.碳元素的原子结构示示意图为 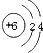 D.碳的相对原子质量为12.01g (2)实验室中,利用下列装置可以制取气体,请回答下列问题. 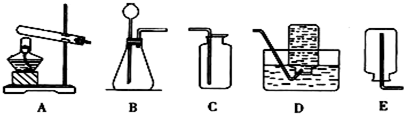 ①用大理石和稀盐酸反应制取CO2,应选用的发生装置是(填代号,下同) B B ,最好选用的收集装置是C C .②加热固体碳酸氢钠和固体碳酸氢铵都能产生CO2,其化学方程式分别是: 2NaHCO3
某同学采用加热固体碳酸氢钠的方法制取CO2,应该选用的发生装置是 A A ,他不选择加热固体碳酸氢铵制取CO2的理由是生成的二氧化碳中混有氨气 生成的二氧化碳中混有氨气 .③A装置中试管口略向下倾斜的原因是 防止水蒸气倒流入试管内使试管炸裂 防止水蒸气倒流入试管内使试管炸裂 .(3)已知二氧化碳能与水反应生成酸.某同学设计了以下实验,验证了这一结论. 实验1:取4朵用石蕊溶液染成紫色的干燥的纸花.往第一朵纸花上喷上稀醋酸,小花变红色. 实验2:往第二朵纸花上喷上水,纸花不变色. 实验3: 实验4:往第四朵纸花上喷水后,再放入盛有CO2的集气瓶中,纸花变红色. 回答下列问题: ①实验2的目的是 证明水不能使紫色石蕊试液变红 证明水不能使紫色石蕊试液变红 ;②请补充实验3: 将第二朵纸花伸入盛有二氧化碳的集气瓶中 将第二朵纸花伸入盛有二氧化碳的集气瓶中 ;③二氧化碳与水反应的化学方程式为 CO2+H2O=H2CO3 CO2+H2O=H2CO3 .(4)称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放入烧杯中,向其中加入50g稀盐酸(盐酸没有消耗完).反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量).试计算石灰石中杂质的质量分数. 查看答案和解析>> 科目:初中化学 来源: 题型: 结构决定性质,性质决定用途。镁元素的原子结构示 意图如右图所示: (1)X的值是 。 (2)镁元素的化学性质与下列 (填选项字母)元素的化学性质相似。
A B C D (3)写出一种含镁元素的化合物的化学式为 。 (4)镁粉可作照明弹,说明镁具有的化学性质是 。 查看答案和解析>> 科目:初中化学 来源: 题型: 下图是元素周期表中1—18号元素的原子结构示 意图,观察下图,探究下列问题:
(1)核外电子是 排布的。第一层电子数不超过 个;第二层电子数不超过 个;最外层电子数不超过 个。 (2)周期数== 。同一周期的元素,① 相同; ② 逐渐递增;③每周期开头的是 类型的元素,靠近尾部的是 类型的元素,结尾的是 类型的元素。 (3)族数== 。同族元素,① 相同; ② 相似;③ 逐渐递增。 (4)填充下表:
(5)最外层为 个电子(只有1个电子层时 个)的结构称为稳定结构。在化学反应中,元素的原子通过得或失电子形成相对稳定结构。 结论:元素的化学性质与 ,特别是 有密切的关系。即 决定元素的化学性质。 查看答案和解析>> 科目:初中化学 来源:2012-2013学年江苏省盐城市景山中学九年级(上)期中化学试卷(解析版) 题型:填空题 据有关资料介绍,儿童缺钙会得佝偻病,成年人缺钙会得软骨病,血液中也有少量钙,它对皮肤伤口血液的凝固起着重要作用. 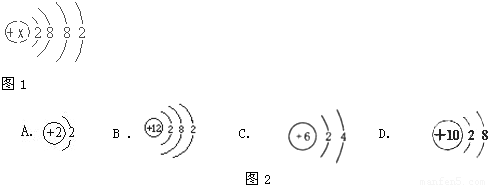 (1)钙原子结构示意图如图所示,该原子的核电荷数为 ,它在元素周期表中位于第 周期;离子符号为 , 它和氯元素形成的化合物的化学式为 (2)钙元素化学性质与下列哪种元素化学性相似 (3)某钙片的标签如下,且知此钙片成分中只有碳酸钙(CaCO3)含有钙元素.
②如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片.请计算每天他需补充碳酸钙多少克? 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |