
| ʵ����� | ��һ�� | �ڶ��� | ������ | ���Ĵ� | ����� |
| ����ϡ��������� | 50g | 50g | 50g | 50g | 50g |
| �ձ����ձ������ʵ������� | 159.1g | 206.9g | 254.7g | 302.5g | 352.5g |
 x=21.2g
x=21.2g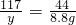 y=23.4g
y=23.4g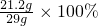 =73.1%
=73.1%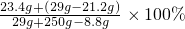 =11.5%
=11.5%

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
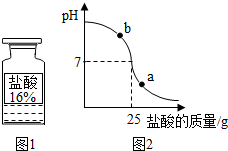 ��2013?�ߴ��ض�ģ��ѧϰ��ѧһ���ͬѧ�ǶԿα��ϡ���Խ�ǿ�Ľ���һ����Խ�λ�������Ľ��������ǵ�����Һ���û��������Լ���֧��ȼ�յ�����һ���������������仰���������ɣ�����ʦ�İ����£��ý�������̽���������⣺
��2013?�ߴ��ض�ģ��ѧϰ��ѧһ���ͬѧ�ǶԿα��ϡ���Խ�ǿ�Ľ���һ����Խ�λ�������Ľ��������ǵ�����Һ���û��������Լ���֧��ȼ�յ�����һ���������������仰���������ɣ�����ʦ�İ����£��ý�������̽���������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��
ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��| �¶�/�� | 0 | 10 | 20 | 30 | 40 | |
| �� �� �� /g |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |

| ��ҵ�������Na 2CO3%�ݣ� | ||
| �ŵ�Ʒ | һ��Ʒ | �ϸ�Ʒ |
| 99.2 | 98.8 | 98.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ӧǰ | ��Ӧ�� | ||
| ʵ������ | ������ˮ��Ʒ������ | ����AgNO3��Һ������ | ���˺�ʣ����Һ������ |
| 130g | 40g | 167.13g | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
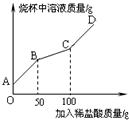 ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��
ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��| �¶�/�� | 0 | 10 | 20 | 30 | 40 | |
| �� �� �� /g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |

| ��ҵ�������Na 2CO3%�ݣ� | ||
| �ŵ�Ʒ | һ��Ʒ | �ϸ�Ʒ |
| 99.2 | 98.8 | 98.0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com