
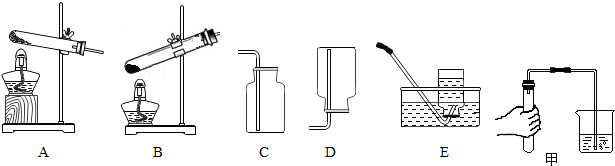
分析 (1)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
氧气的密度比空气的密度大,不易溶于水;排水法收集气体的适宜时机是集气瓶口气泡连续、均匀冒出时;
(2)据检查装置气密性的方法分析解答
(3)氧气能够支持燃烧,能使带火星的木条复燃,据此验满;
(4)如果操作不当,会影响实验结果,甚至会导致实验失败,结合加热固体的注意事项分析解答;
(5)根据质量守恒定律:反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算反应的氯酸钾的质量.
解答 解:(1)用氯酸钾和二氧化锰制备氧气需要加热,应选用的气体发生装置是A,选择依据是:反应物是固体,反应需要加热,加热固体时试管口要下倾,防止冷凝水倒流引起试管炸裂;反应方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;选用装置E来收集氧气,其原因是氧气不易溶于水;
(2)如果装置不漏气,可以看到导管口有气泡冒出,将手松开一段时间后(导管仍插入水中),可以看到的现象是:导管中进入一段水柱,因为内外产生了压强差;
(3)若选用C收集氧气,验满的方法是:把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(4)如果没有预热,加热时试管外壁有水,试管触及灯芯,实验结束拆除装置时先熄灭酒精灯等,都能够导致试管炸裂;
(5)①设反应的氯酸钾的质量为x,
②反应生成氧气的质量为:30g-20.4g=9.6g,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{96}$=$\frac{x}{9.6g}$
x=24.5g,
故答案为:(1)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;氧气不易溶于水;气泡连续均匀冒出时;
(2)导管内进入一段水柱;
(3)把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满;
(4)试管触及灯芯(合理即可);
(5)答:①生成氧气的质量是9.6g.
②原混合物中氯酸钾的质量是24.5g.
点评 本考点主要考查了检查装置的气密性、气体的制取装的选择,验满,同时也考查了方程式的书写和计算等,综合性比较强.解答时要结合所学知识细心分析解答.


科目:初中化学 来源: 题型:推断题
 如图所示,现有甲、乙、丙、X、Y、Z六种初中化学常见物质,其中连线两端的物质间能发生反应;箭头两端的物质只通过一步反应就能实现转化.已知X、Y、Z都含有同一种元素,且X和Y是组成元素相同的无色液体;甲、乙、丙属于不同类别的物质,其中甲是胃酸的成分,乙的悬浊液常用来涂刷树木以防虫害.则:
如图所示,现有甲、乙、丙、X、Y、Z六种初中化学常见物质,其中连线两端的物质间能发生反应;箭头两端的物质只通过一步反应就能实现转化.已知X、Y、Z都含有同一种元素,且X和Y是组成元素相同的无色液体;甲、乙、丙属于不同类别的物质,其中甲是胃酸的成分,乙的悬浊液常用来涂刷树木以防虫害.则:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硬水、软水--加肥皂水,搅拌观察泡沫的多少 | |
| B. | 羊毛纤维、涤纶--灼烧,闻气味 | |
| C. | 氢氧化钠、氢氧化镁--加水观察 | |
| D. | 氯化钠、氢氧化钠--加稀盐酸区分 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
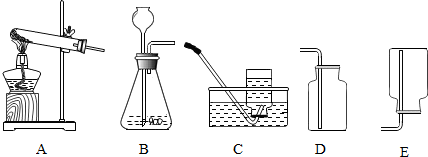
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
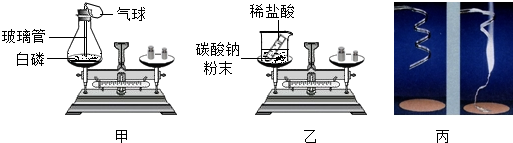
| 实验现象 | |||
| 甲同学 | ①白磷燃烧,产生浓浓的白烟,放出热量,气球先变大后又变小,天平平衡 | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 该反应遵守质量守恒定律 |
| 乙同学 | ②烧杯内产生大量气泡,天平不平衡 | ③Na2CO3+2HCl=2NaCl+H2O+CO2↑ | 该反应遵守质量守恒定律 |
| 丙同学 | 镁条剧烈燃烧,发出耀眼白光,放热,生成 白色固体.反应前后称量质量不相等. | ④2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该反应不遵守质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
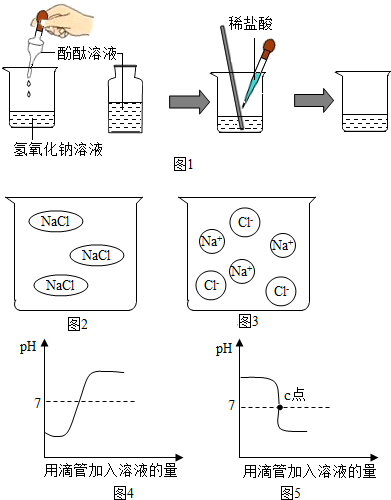 据图填空.
据图填空.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 两种物质相互反应生成盐和水,证明该反应是中和反应 | |
| B. | 一定温度下,往氢氧化钙饱和溶液中加入氧化钙,再恢复到原温度,则原溶液中溶质、溶剂的质量一定改交 | |
| C. | 在同一化合物中,金属元素一定显正价,非金属元素一定显负价 | |
| D. | 某物质在空气中燃烧生成二氧化碳和水,证明该物质含碳、氢、氧三种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com