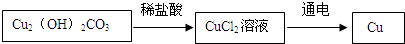
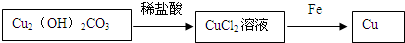
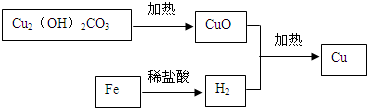
碱式碳酸铜是一种绿色的固体,受热分解成黑色固体物质、二氧化碳和水.这种黑色固体的成分是什么呢?亮亮与间学们进行以下探究:
[猜想]:该黑色固体可能氧化铜,也可能是氧化铜和炭的混合物.
[设计与实验]
| 实验步骤 |
实验现象 |
结论和化学方程式 |
| 亮亮同学取少量黑色固体,放入试管中,加入足量的稀硫酸,微热. |
黑色固体完全消失,溶液变 蓝 蓝 色. |
此黑色固体是氧化铜.该反应的化学方程式为 CuO+H2SO4═CuSO4+H2O CuO+H2SO4═CuSO4+H2O |
接着小明与同学们用氢气还原氧化铜制取铜.
(1)要制得纯净的氢气,小明应选用的药品是
D
D
A、铁和稀硫酸 B、锌和浓盐酸 C、镁和稀硫酸D、锌和稀硫酸
(2)实验开始时,应先通入一会儿
H2
H2
,然后再加热,这样操作的目的是
防止加热时发生爆炸
防止加热时发生爆炸
(3)实验结束后,小方同学对还原后的红色物质产生了兴趣,该红色物质一定是单质铜吗?
查阅有关资料获知:氢气与氧化铜在加热条件下能生成氧化亚铜(Cu
2O),氧化亚铜也呈红色,且能与稀硫酸反应生成硫酸铜、铜和水.
为此,小方同学靠后做了两次实验,第一次称取4.0g氧化铜进行实验,得到了3.3g红色物质;第二次同样用4.0g氧化铜进行实验,得到了3.2g红色物质.
①小方通过对所得实验数据迸行计算分析后知t第二次实验得到的红色物质全部是铜,第一次得到的红色物质除铜外,还含有氧化亚铜.小方的分析依据是
4gCuO中含有的铜元素质量为3.2g,所以生成铜的质量为3.2g
4gCuO中含有的铜元素质量为3.2g,所以生成铜的质量为3.2g
.
②随后,他用化学实验方法验证了上述分析结果的正确性.其验证方法是(简要写出操作现象、结论)
分别取两种红色固体于试管中,加入稀硫酸.第一次试管中溶液变蓝,第二次试管中溶液不变蓝,则第一次的产物中含有氧化亚铜,第二次的是铜
分别取两种红色固体于试管中,加入稀硫酸.第一次试管中溶液变蓝,第二次试管中溶液不变蓝,则第一次的产物中含有氧化亚铜,第二次的是铜
③从上述实验中,小方获得以下结论:在氢气还原氧化铜实验中,若还原不充分,一会得到红色氧化亚铜,请写出氢气还原氧化铜生成氧化亚铜的化学方程式
.



 习题精选系列答案
习题精选系列答案
 (2012?烟台)2012年3月6日,包括圆明园兽首在内的一批珍贵文物首次在烟台展出.小霞看到这些240年前的铜质兽首后,她想探究铜是怎么冶炼出来的.
(2012?烟台)2012年3月6日,包括圆明园兽首在内的一批珍贵文物首次在烟台展出.小霞看到这些240年前的铜质兽首后,她想探究铜是怎么冶炼出来的.