
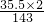 ×100%=49.7%.
×100%=49.7%.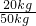 ×250g=100g.
×250g=100g.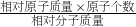 ×100%,进行分析解答.
×100%,进行分析解答.

 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案科目:初中化学 来源: 题型:阅读理解
| 方便面营养成分表(每100g中含量) | |||||||||
| 糖类 (g) |
脂肪 (g) |
蛋白质 (g) |
水分 (g) |
钠 (mg) |
钾 (mg) |
磷 (mg) |
钙 (mg) |
维生素C (mg) |
其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 玉树发生了大地震,全国人民抗震救灾,众志成城,彰显了中华民族的巨大凝聚力.请回答下列问题:
玉树发生了大地震,全国人民抗震救灾,众志成城,彰显了中华民族的巨大凝聚力.请回答下列问题:| 方便面营养成分表(每100g中的含量) | |||||||||
| 糖类/g | 脂肪/g | 蛋白质/g | 水分/g | 钠/mg | 钾/mg | 磷/mg | 钙/mg | 维生素C/mg | 其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
查看答案和解析>>
科目:初中化学 来源:2012年云南省曲靖市马龙县通泉中学中考化学模拟试卷(三)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com