
【题目】为测定某BaCl2溶液的溶质质量分数,现取100gBaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,(反应方程式:BaCl2+H2SO4=BaSO4 ↓+2HCl)请回答:
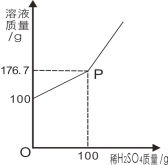
(1)P点意义_______________。
(2)反应生成BaSO4沉淀的质量为_________g。
(3)求原BaCl2溶液的溶质质量分数。
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:
【题目】(7分)化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
【提供资料】① 二氧化碳与过氧化钠反应生成氧气和另一种物质。
②Na2O2是一种淡黄色固体,常温下能与H2O、HCl气体等物质发生反应,生成氧气不能与N2发生反应。
(1)探究二氧化碳与过氧化钠反应生成氧气。
同学们在老师的指导下设计了如下图所示装置。
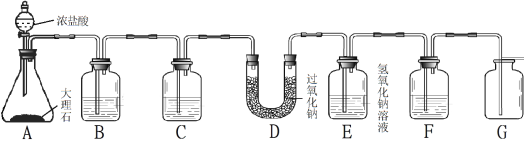
① 写出检验G中气体的方法 。
②若无装置C,对实验有影响的物质是 。
③若观察到 ,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
【猜想与假设】下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
你认为猜想 是不正确的,理由是 。
【进行实验】排除错误猜想后,同学们通过以下实验验证了另一种物质。
实验操作 | 实验现象 |
取少量CO2与Na2O2反应后的固体于试管中,加入稀盐酸。 | 有大量气泡产生 |
【反思与评价】
①某同学认为上述方案存在不足,他的理由是 。
②写出过氧化钠与二氧化碳反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶无色气体,可能是氧气或二氧化碳,完成下列问题。
操作 | 现象 | 结论 |
将_________________伸入集气瓶中 | ________________________ | 这瓶气体是氧气 |
向集气瓶中滴加适量________,振荡 | ________________________ | 这瓶气体是 二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分) 科技节活动中,化学实验小组做了如下实验,请回答以下问题.
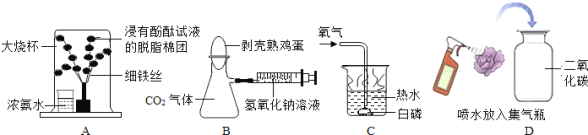
(1)图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为
色,该实验中没有涉及的性质是 (填字母).
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
(2)图B所示实验,将注射器中浓氢氧化钠溶液注入瓶中,会看到鸡蛋被“吞”入瓶中,该实验中涉及的化学方程式为
(3)图C所示实验,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②达到燃烧所需要的 ③ .
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是
(用化学方程式表示).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
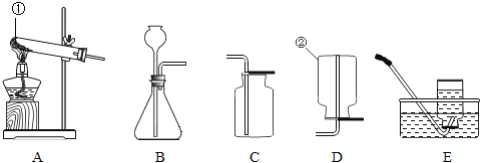
(1)写出指定仪器的名称:① ;
(2)实验室用无水醋酸钠固体、碱石灰共热制取密度比空气小、难溶于水的甲烷,可选用的发生装置是 (选填字母,下同),可选用的收集装置是 。
(3)实验室可用B、E装置制取的气体是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有关下列的各种描述中,属于物质的物理性质的是( )
A.氧气能支持燃烧
B.氧气是一种无色、无味的气体
C.氢气能燃烧
D.过氧化氢在加热时能产生氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液。请回答下列问题;
(1)配制步骤
①计算:需氢氧化钠固体 g,水960mL(水的密度是1 g/cm3)。
②称量:用质量为23.1 g的烧杯作称量容器,托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在左盘。
③溶解:将氢氧化钠固体溶于水,用玻璃棒搅拌,使氢氧化钠全部溶解,冷却至室温。
④装瓶:把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
请在装有所配制溶液的试剂瓶(见下图)标签上标明相应的信息。

(2)配制过程,导致溶液中氢氧化钠质量分数小于4%的可能原因是
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③用托盘天平称取氢氧化钠,将氢氧化钠放置在右盘;④盛装溶液的试剂瓶用蒸馏水润洗;⑤氢氧化钠固体不纯。
(3)若老师提供的药品有500 g 8%的氢氧化钠溶液,500 g 1%的氢氧化钠溶液,足量的氢氧化钠固体和水,除了上述配制方案外,你还可以设计出哪些配制方案,请你写出其中的一种: .(只要说明配制时所需的各种药品及用量即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com