
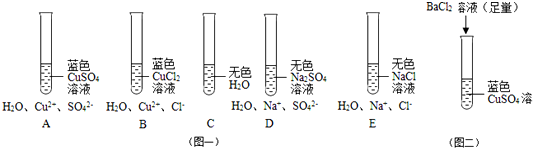
分析 根据题意,在稀溶液中SO42-、Cl-呈无色;想用实验证明CuSO4溶液显蓝色是由什么微粒造成的,可以采用对比实验的方法,根据对比实验设计的一般思路,比较A、B、C、D、E五支试管中所盛试剂的颜色与所含微粒,进行分析解答即可.
解答 解:根据A、B、C三支试管中所盛试剂的颜色与所含微粒,水是无色的,A、B的溶液中均含Cu2+,均显蓝色,说明Cu2+的存在使CuSO4、CuCl2溶液显蓝色.
D、E两支试管中均含钠离子,根据题意,在稀溶液中SO42-、Cl-呈无色,说明在水溶液中,Na+是无色的.
根据对A、D的分析,A、D的溶液中均含水分子、硫酸根离子,水分子不能使溶液显蓝色,在稀溶液中SO42-呈无色,说明A中是Cu2+使CuSO4溶液显蓝色.
选择一种试剂与CuSO4溶液反应,保持溶液中Cu2+ 的存在,可选用氯化钡与硫酸铜反应,反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2.
如图二所示的方法是除去溶液中的Cu2+,是氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
故答案为:
(1)Cu2+;
(2)D、E;
CuSO4+BaCl2=BaSO4↓+CuCl2;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
点评 本题难度较大,考查同学们用不同的思维方式、用对比实验设计的一般思路、从不同的切入点研究同一个问题的能力,培养了学生的综合能力.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:初中化学 来源: 题型:解答题
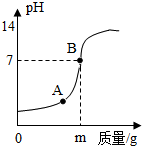 向某盐酸中不断加入氢氧化钠固体时,溶液的pH与加入的氢氧化钠固体质量关系如图所示.当溶液的pH处于A点时,溶液中所含有的粒子为氢离子、氯离子、水分子、钠离子( 多填、少填均不得分);当溶液的pH处于B点时,向溶液中滴加紫色石蕊试液,溶液呈紫色;若改用m 克消石灰与该盐酸充分反应,所得溶液的pH>7(填“>”、“=”、“<”).
向某盐酸中不断加入氢氧化钠固体时,溶液的pH与加入的氢氧化钠固体质量关系如图所示.当溶液的pH处于A点时,溶液中所含有的粒子为氢离子、氯离子、水分子、钠离子( 多填、少填均不得分);当溶液的pH处于B点时,向溶液中滴加紫色石蕊试液,溶液呈紫色;若改用m 克消石灰与该盐酸充分反应,所得溶液的pH>7(填“>”、“=”、“<”).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 体温计热胀冷缩,是因为原子间的间隔发生了改变• | |
| B. | 走进家门能闻到菜的香味,是因为分子在不断地运动 | |
| C. | 不同的花儿有不同的香味,是因为不同的分子性质不同 | |
| D. | 保温瓶刚灌入开水时瓶塞很容易被顶起,是由于水分子受热膨胀变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 烧杯中盛有CaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有CaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段产生白色沉淀 | |
| B. | bc段溶液质量增加106.0g | |
| C. | c点对应溶液的溶质质量分数为7.5% | |
| D. | d点溶液中含有2种溶质,滴加酚酞呈红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 催化剂在化学反应前后其化学性质发生了变化 | |
| B. | 高炉炼铁产物是生铁,其含碳量为0.03%-2% | |
| C. | 硝酸铵溶解在水中,溶液温度会升高 | |
| D. | 动植物的新陈代谢过程中有物质的缓慢氧化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
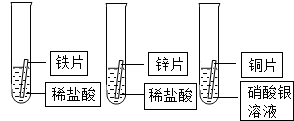
| 实验步骤 | 实验现象 | 实验结论 |
| 将用砂纸打磨过的铁片浸入硫酸铜溶液中,仔细观察 | 铁片表面有红色固体附着 | 铁的活动性比铜强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com