
【题目】(7分)A~N是初中学过的物质。D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。(注:难溶性碱加热分解生成对应的氧化物)
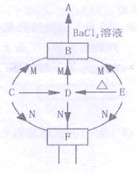
(1)写出化学式:A ,N 。
(2)写出E→B的化学反应方程式 。
(3)由F生成E需加入的物质是 。
(4)C在空气中燃烧生成D的实验现象是 。C在空气中燃烧除了生成D 之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3),该氮化物的化学式是 。
【答案】(1)BaSO4 HCl (2)Mg(OH)2+H2SO4 = MgSO4+2H2O
(3)NaOH或KOH等 (4)发出耀眼的白光,产生白烟,生成白色固体 Mg3N2
【解析】
试题分析:D是相对分子质量为40的氧化物说明D是氧化镁,因此C是镁,C在空气中燃烧生成D的实验现象是发出耀眼的白光,产生白烟,生成白色固体,C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3),因为镁的化合价为+2价,所以该氮化物的化学式是Mg3N2;实验室通常用N制取CO2且D能够和N反应,说明N是盐酸,A是物质和氯化钡反应的结果,所以A是硫酸钡沉淀,E是难溶于水的白色沉淀,且加热会产生氧化镁,所以E是氢氧化镁,B是E获得的使用B是硫酸镁,因此写出E→B的化学反应方程式Mg(OH)2+H2SO4 = MgSO4+2H2O;F是由D和N反应获得,所以F是氯化镁,由F生成E需加入的物质是一种可溶性的碱,所以需加入的物质是NaOH或KOH等。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:
【题目】下列离子能在pH=11的溶液中大量共存的是
A、K+、NO3-、Na+、OH- B、CO32-、K+、Cl-、Ca2+
C、H+、Ba2+、Cl-、SO42- D、K+、OH-、SO42-、Cu2+
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式表示的反应,符合实验事实的是
A.Cu+2HCl == CuCl2 +H2↑ B.Zn+2 AgCl == ZnCl2 + Ag
C.Fe +ZnSO4 ==FeSO4 + Zn D.Cu +Hg(NO3)2== Cu(NO3)2 +Hg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)有关NaOH与CO2反应的探究
探究一:检验NaOH固体样品露置空气中一段时间后的成分
【查阅资料】Na2CO3溶液是碱性;KCl溶液、BaCl2溶液显中性、BaCO3难溶于水。
(1)检验样品是否变质。检验样品成分中是否含碳酸根的实验方法(操作、现象及结论):________________。
(2)检验样品是否完全变质。实验操作:取样品加水溶解,先加过量的_________(填编号,下同),再滴加________。
A.盐酸
B.KCl溶液
C.BaCl2溶液
D.Ba(OH)2溶液
E.酚酞试液
探究二:用NaOH溶液测定空气中酸性气体(CO2、SO2)的体积分数
【实验装置】如图8所示,向细玻璃管内注入少量水,形成一段水柱;经检查该装置气密性良好。已知细玻璃管单位长度的容积为0.1mL·cm—1。水柱的质量忽略不计。

【操作步骤】保持外界条件不变,完成以下操作:
①将40mL浓NaOH溶液迅速倒入烧瓶内,立即塞紧橡皮塞,并在细玻璃管上标记水柱底部的位置
②观察并测量得出水柱缓慢向下移动的距离为2.0cm;
③实验结束后,根据①中的标记,测得该标记以下细玻璃管及烧瓶的总容积为340mL。
(3)检查图8装置气密性的操作方法:________________________________________。
(4)仅根据本次测量数据,该气体样品中酸性气体的体积分数为________(精确到0.00001)。
(5)在上述操作步骤②中,若装置温度略有升高,实验结果______(填“偏大”、“不变”或“偏小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)回答实验室用高锰酸钾制取氧气的相关问题。
(1)写出制取原理的化学方程式:__________________________。
(2)如下图所示,发生装置应选用_____________(填编号,下同),以下气体收集装置不能采用的是_____________。
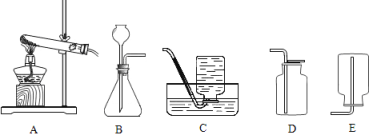
(3)为测定高锰酸钾分解生成氧气的体积,应选用下图装置_____________(填编号)。
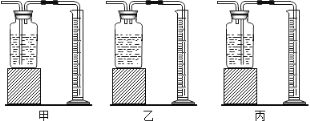
(4)实验结束,某同学发现收集到的纯氧气质量大于通过化学方程式计算所得质量。不考虑实验误差,请你就此提出一种猜想并设计相应验证方案:_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)现代循环经济要求综合考虑环境污染和经济效益。高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:[(NH4)2CO3溶液呈碱性,40 ℃以上时(NH4)2CO3分解]。
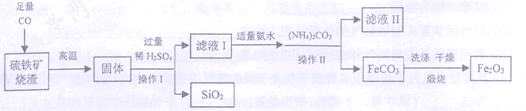
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、 等。
(2)滤液Ⅰ中主要的阳离子是 等。
(3)加适量氨水的目的是 。
(4)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是 。
(5)滤液Ⅱ中可回收的产品是 (写化学式)。
(6)写出在空气中煅烧FeCO3的化学反应方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列括号中对日常生活的变化判断正确的是
A.水蒸发(化学变化) B.鞭炮爆炸(化学变化)
C.食物腐烂(物理变化) D.烧鱼时把鱼烧焦(物理变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com