将28克不纯的铁(杂质不与酸反应)跟足量的硫酸充分反应,反应后收集到0.9克氢气,求该不纯的铁中杂质的质量分数.
【答案】
分析:根据铁与硫酸反应的化学反应方程式,将氢气的质量代入化学反应方程式来计算铁的质量,再计算该不纯的铁中杂质的质量分数.
解答:解:因杂质不与酸反应,则产生的气体是铁与酸反应生成的,
设铁的质量为x,
则Fe+2H
2SO
4═FeSO
4+H
2↑
56 2
x 0.9g

,
解得x=25.2g,
则杂质的质量为28g-25.2g=2.8g,
则杂质的质量分数为
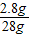
×100%=10%,
答:该不纯的铁中杂质的质量分数为10%.
点评:本题考查学生利用化学反应方程式的计算,将气体的质量直接代入计算即可,应注意最后计算的是杂质的质量分数,易计算为铁的质量分数而出错.

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案