
 酸、碱、盐是重要的化合物,研究它们的性质有重要意义.
酸、碱、盐是重要的化合物,研究它们的性质有重要意义.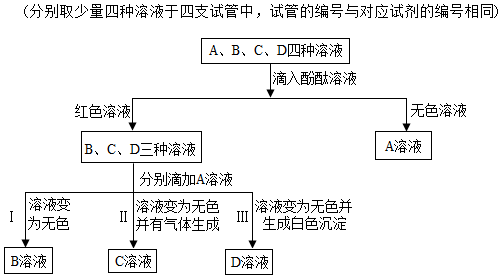
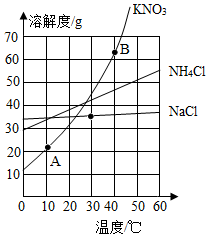
分析 (1)根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的;
(2)根据氢氧化钠、氢氧化钾属于碱,碳酸钠溶液显碱性,能使酚酞变红色,碳酸盐会与钡离子反应生成碳酸钡沉淀,会与酸反应生成二氧化碳气体等知识进行分析.
解答 解:(1)①通过分析溶解度曲线可知,三种固体物质的溶解度受温度影响最小的是氯化钠;
②30℃时,硝酸钾的溶解度最大,氯化铵次之,氯化钠的溶解度最小,所以三种固体物质饱和水溶液中溶质的质量分数由大到小的顺序是:硝酸钾、氯化铵、氯化钠;
③图中A、B点的坐标为:A(10,21)、B(40,64),
设40℃100g硝酸钾饱和溶液中溶质质量为x
100:x=(100g+64g):64g
x=39g
所以溶剂质量为:100g-39g=61g,
设61g水在10℃时最多溶解硝酸钾的质量为y
100:21=61:y
y=12.81g
所以析出KNO3固体的质量为:39g-12.8g=26.2g;
(2)A、B、C、D四种溶液中滴入酚酞,A溶液显无色,所以A是稀硫酸,B、C、D是氢氧化钡、氢氧化钠、碳酸钠中的一种,滴加稀硫酸,C溶液变为无色,有气泡产生,所以C是碳酸钠,D溶液变为无色,并产生白色沉淀,所以D是氢氧化钡,B溶液变为无色,所以B是氢氧化钠,所以
①反应Ⅲ是氢氧化钡和硫酸反应生成硫酸钡沉淀和水,化学方程式为:Ba(OH)2+H2SO4=BaSO4↓+2H2O;
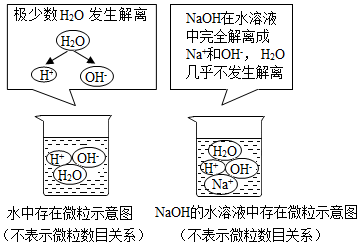
②通过分析题中的微观图示,水中含有氢离子和氢氧根离子,水显中性;氢氧化钠溶液中含有钠离子、氢氧根离子、氢离子,所以C溶液能使酚酞溶液变红的原因是氢氧根离子的数目大于氢离子的数目,故选:d.
故答案为:(1)①氯化钠;
②硝酸钾、氯化铵、氯化钠;
③26.2;
(2)①Ba(OH)2+H2SO4=BaSO4↓+2H2O;
②d.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 除去铁制品表面的铁锈,用过量的稀硫酸长时间浸泡 | |
| B. | 验证甲烷中含有H2,点燃,在火焰上方罩一只干冷烧杯,观察内壁是否出现液滴 | |
| C. | 鉴别化肥KNO3和NH4Cl,取样与熟石灰混合研磨,闻气味 | |
| D. | 检验NaOH是否变质,取样,加水溶解后滴加酚酞试液,观察溶液颜色是否变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
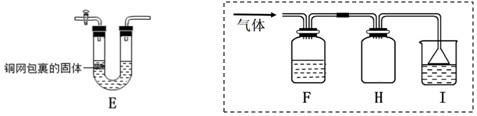
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com