
 C2H2+3H2
C2H2+3H2



科目:初中化学 来源: 题型:阅读理解
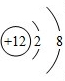
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
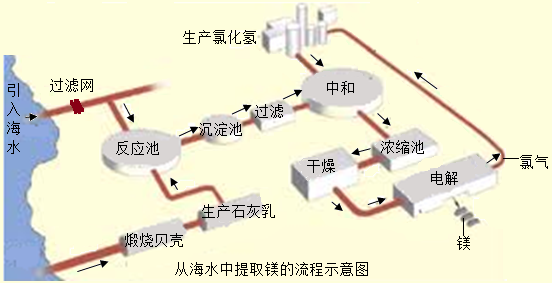
镁合金的强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉。海水提镁是国际上的主要趋势,工业流程图如下:

其步骤为:
I.将海边大量存在的贝壳(主要成分为CaCO3煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2·6H2O
Ⅳ.将MgCl2·6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg(1)请根据上述步骤回答问题:
①写出步骤I、Ⅲ的有关化学方程式:
I.贝壳煅烧成生石灰 ;
Ⅲ.Mg(OH)2沉淀中加入盐酸中和 。
②步骤I~V中有分解反应的是(填写步骤序号): 。
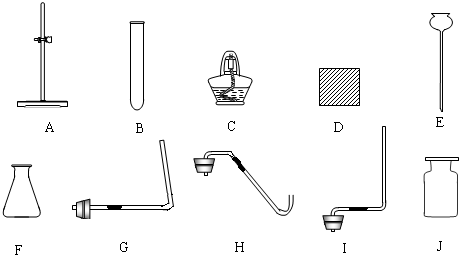
③步骤11中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发需要的主要仪器有 、 、酒精灯、带铁圈的铁架台、坩埚钳等。
④上述海水提镁的流程中,采取了哪些措施来降低成本、减少污染的?请写出其中一点:
。
(2)回答下列问题:
①右图为镁元素的某种粒子结构示意图,该图表示(填序号)

A.分子 B.原子 C.阳离子D.阴离子.
②镁原子在化学反应中容易失去电子,镁是一种(填“活泼”或”不活泼”) 金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应。
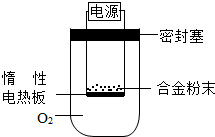
 (3)为测定约含镁30%的镁铝合金(不含其它元素)中镁的质量分数。 ①第一小组设计下列实验方案:称量a g镁铝合金粉末,放在如右图所示装置的惰性电热板上,通电使其充分灼烧。
(3)为测定约含镁30%的镁铝合金(不含其它元素)中镁的质量分数。 ①第一小组设计下列实验方案:称量a g镁铝合金粉末,放在如右图所示装置的惰性电热板上,通电使其充分灼烧。
讨论一:欲计算镁的质量分数,该实验中还需测定的一种数据是 。
讨论二:若用空气代替O2进行实验,对测定结果(填“有”或“无”) 影响。
②第二小组设计下列实验方案:称取b g镁铝合金,与足量的稀盐酸完全反应。
欲计算镁的质量分数,该实验中还需测定的一种数据是 。
查看答案和解析>>
科目:初中化学 来源:2010年黑龙江省哈尔滨市中考化学模拟试卷(三)(解析版) 题型:解答题
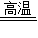 C2H2+3H2
C2H2+3H2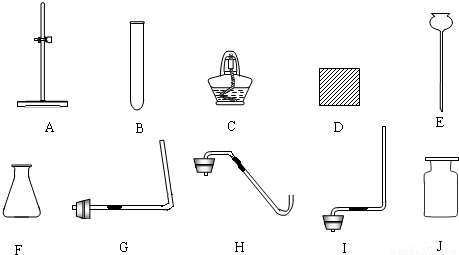
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com