解:(1)因制取三种气体时可以不用加热,可以不使用催化剂,在制取二氧化碳和氢气时反应物有混合物,且制取气体要保证气体纯净,则应没有气体参加反应,还应只生成一种气体才可以,故答案为:③⑤;
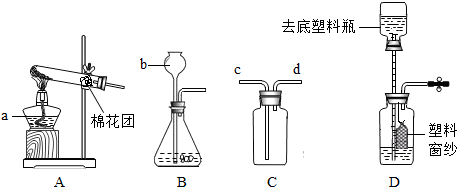
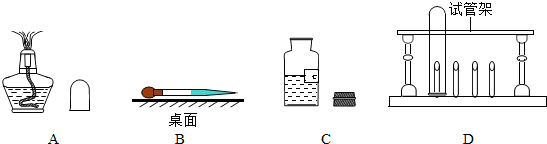
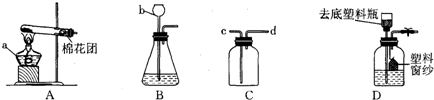
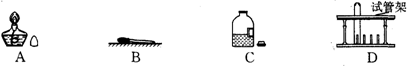
(2)由图可知a是铁架台,c是集气瓶,d是烧杯可以用来溶解固体或在烧杯中稀释液体等,故答案为:铁架台;集气瓶;溶解固体;
(3)因②中生成两种气体,则不可用来制取氨气,若选择①,则是固体加热装置,需选择仪器abf,若选择③,则是固液反应装置,需选择仪器bh,又氨气的密度比空气的小,氨气能溶于水,则可采用向下排空气法收集,由反应原理,若为固体加热装置还可以用来制取氧气,若为固液反应装置,可以用来制取二氧化碳或氢气等,故答案为:①或③;abf或bh;向下排空气法;O
2或CO
2、H
2;
(4)问题一:因双氧水和二氧化锰制氧气时生成水和氧气,则发生反应的化学反应方程式为2H
2O
2
2H
2O+O
2↑,故答案为:2H
2O
2
2H
2O+O
2↑(或用Fe
2O
3做催化剂);
问题二:根据反应能生成氧气判断,MnO
2和 Fe
2O
3在上述反应中质量不变,则其作用是催化作用;为了实验目的准确性,反应过快不利用气体的收集,则实验②③中的H
2O
2的浓度(w%)以 5%为宜,故答案为:催化作用;5%;
问题三:由比较二氧化锰和氧化铁的催化作用,可得出在相同条件下,MnO
2的催化效果好;,比较不同质量分数发生过氧化氢溶液生成氢气的速率,可得出H
2O
2浓度越大,产生氧气的速度越快,答:在相同条件下,MnO
2的催化效果比 Fe
2O
3好;在其他条件相同的情况下,H
2O
2浓度越大,产生氧气的速度越快.
分析:(1)根据实验室制取O
2、CO
2、H
2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法来分析共性;
(2)根据常见仪器及仪器的名称、仪器的用途来分析解答;
(3)根据不同反应原理来选择不同的反应装置,利用气体的性质来选择收集方法,并利用不同气体的反应原理的相似之处来选择同一装置;
(4)问题一、根据反应物和反应规律书写化学方程式;
问题二、从对比实验的结果分析回答;
问题三、从反应速度和溶液中溶质的质量分数的不同分析.
点评:本题考查的知识点较多,学生应学会对实验进行归纳与比较,能根据实验中的数据和信息,正确的分析问题,解决问题,从而得出准确答案.


 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O 2H2O+O2↑,故答案为:2H2O2
2H2O+O2↑,故答案为:2H2O2 2H2O+O2↑(或用Fe2O3做催化剂);
2H2O+O2↑(或用Fe2O3做催化剂);

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案