

分析 (1)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,会看到铁锈消失,溶液呈黄色,写出反应的化学方程式即可;待铁锈消失后,铁与稀盐酸反应生成氯化亚铁和氢气.
(2)高钙豆奶粉的“钙”指的是钙元素,二氧化碳的固体叫干冰,干冰可以进行人工降雨,也可以做制冷剂等;
解答 解:(1)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,会看到铁锈消失,溶液呈黄色,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;待铁锈消失后,铁与稀盐酸反应生成氯化亚铁和氢气,会看到有气泡产生.反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
(2)高钙豆奶粉的“钙”指的是钙元素,二氧化碳的固体叫干冰,干冰可以进行人工降雨,也可以做制冷剂等;
故答案为:(1)Fe2O3+6HCl═2FeCl3+3H2O;有气泡产生;Fe+2HCl═FeCl2+H2↑;(2)元素; 人工降雨;
点评 本题难度不大,掌握铁锈的主要成分、酸的化学性质等并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
 汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.
汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量 | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 200 | 100 |
| 反应后过滤,得干燥固体的质量/g | 4 | 4 | 13 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
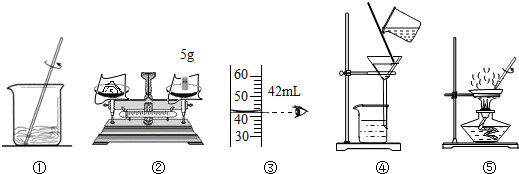
| A. | 甲实验的步骤是①④⑤,其中去除杂质的关键一步是蒸发 | |
| B. | 乙实验按照②③①的步骤进行操作,会导致配制的溶液浓度偏小 | |
| C. | 甲实验各步操作中的玻璃棒都是用来搅拌的 | |
| D. | 乙实验中,若①所用烧杯刚用清水洗过,其他步骤均正确,则配制的溶液浓度偏大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
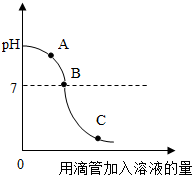
 化学小组为测定Na2CO3和NaCl混合物中Na2CO3的质量分数,同学取样品15g,加入100g水完全溶解后,向其中加入CaCl2溶液,测得溶液质量增量与加入CaCl2溶液的质量关系如图所示.求:
化学小组为测定Na2CO3和NaCl混合物中Na2CO3的质量分数,同学取样品15g,加入100g水完全溶解后,向其中加入CaCl2溶液,测得溶液质量增量与加入CaCl2溶液的质量关系如图所示.求:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 所得溶液中可能含有Cu2+ | |
| B. | 所得滤渣中可能含有铜和锌 | |
| C. | 所得滤液中一定含有Ag+、Zn2+、Cu2+ | |
| D. | 所得滤渣中一定含有银和铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com