
 已知CaCl2+Na2CO3=CaCO3↓+2NaCl.将15g CaCl2溶液逐滴加入到20g Na2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.若将反应后的物质过滤,蒸干滤液后得到固体的质量是多少.
已知CaCl2+Na2CO3=CaCO3↓+2NaCl.将15g CaCl2溶液逐滴加入到20g Na2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量关系如图所示.若将反应后的物质过滤,蒸干滤液后得到固体的质量是多少. | 111 |
| x |
| 100 |
| 2g |
| 117 |
| z |
| 2.22g |
| 10g |


科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:

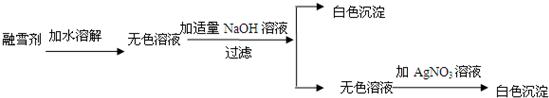
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.
某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶 解 度 /g |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |

| 工业纯碱标准(Na 2CO3%≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2 | 98.8 | 98.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 稀盐酸(或稀硫酸) 稀盐酸(或稀硫酸) |
产生大量的气泡 | 该溶液是 碳酸钠溶液 碳酸钠溶液 ,反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2013?如东县模拟)实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
(2013?如东县模拟)实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 步骤一:取样品于试管中,滴加足量 稀盐酸 稀盐酸 |
产生大量的气泡 | 猜想①正确. 步骤一发生反应的化学方程式是 Na2CO3+2HCl═2NaCl+CO2↑+H2O Na2CO3+2HCl═2NaCl+CO2↑+H2O |
| 步骤二:把产生的气体,通入 澄清石灰水 澄清石灰水 |
石灰水变浑浊 石灰水变浑浊 |
| 探究步骤 | 预计现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的 CaCl2(或BaCl2等) CaCl2(或BaCl2等) 溶液并过滤 |
产生白色沉淀 | 溶液中: 既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变 红 红 色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com