
 4Fe+3CO2↑或者为:Fe2O3+3C
4Fe+3CO2↑或者为:Fe2O3+3C 2Fe+3CO↑
2Fe+3CO↑ 4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克? .
4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克? .
 4Fe+3CO2↑
4Fe+3CO2↑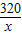 =
= x=3.78g
x=3.78g =
= y=0.42g
y=0.42g 2Fe+3CO↑
2Fe+3CO↑ =
=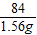 x=2.97g
x=2.97g =
= y=0.66g
y=0.66g ×100%+20m×
×100%+20m× ×100% 29m=72%
×100% 29m=72% 4FeO+CO2↑
4FeO+CO2↑ =
= y=
y=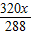
 =
= z=
z=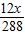
 )=9:20,解得x=144g
)=9:20,解得x=144g =6g
=6g

科目:初中化学 来源: 题型:
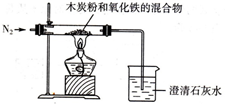 已知木炭粉和Fe2O3反应的化学方程式:2Fe2O3+3C
已知木炭粉和Fe2O3反应的化学方程式:2Fe2O3+3C
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
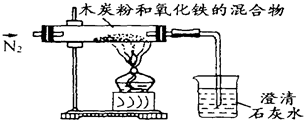 已知木炭粉和Fe2O3 反应的化学方程式为:2Fe2O3+3C
已知木炭粉和Fe2O3 反应的化学方程式为:2Fe2O3+3C
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知木炭粉和Fe2O3 反应的化学方程式为:2Fe2O3+3C
已知木炭粉和Fe2O3 反应的化学方程式为:2Fe2O3+3C 4Fe+3CO2↑或者为:Fe2O3+3C
4Fe+3CO2↑或者为:Fe2O3+3C 2Fe+3CO↑
2Fe+3CO↑ 4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克?______.
4FeO十CO2↑,为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入碳多少克?______.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知木炭粉和Fe2O3反应的化学方程式:2Fe2O3+3C
已知木炭粉和Fe2O3反应的化学方程式:2Fe2O3+3C 4Fe+CO2↑,某同学设计了一个实验,证明氧化铁中含有氧元素,并测定氧化铁中氧元素的质量分数,实验装置如图.
4Fe+CO2↑,某同学设计了一个实验,证明氧化铁中含有氧元素,并测定氧化铁中氧元素的质量分数,实验装置如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com