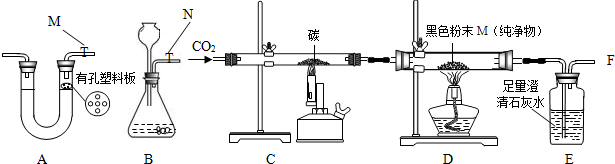
(2012?虹口区一模)某班级同学对实验室制取二氧化碳的若干问题进行如下探究
实验一:实验室制取二氧化碳的原料的选择,实验内容和现象记录如下
实验
步骤 |
 |
 |
 |
| 现象 |
剧烈反应,产生大量气泡,反应迅速停止 |
产生气泡,速率迅速减慢,反应几乎停止. |
产生气泡,反应持续时间较长 |
| 分析 |
反应速率过快,气体不便收集 |
无法持续产生CO2 |
速率适中,便于收集气体 速率适中,便于收集气体 |
| 结论 |
实验室制取二氧化碳的原料是 块状大理石和稀盐酸 块状大理石和稀盐酸 . |
实验二:设计实验发生装置和收集装置
①如图1所示是制取和收集二氧化碳的装置,其中气体发生装置的适用范围是
常温、固液反应
常温、固液反应
,集气瓶中导管应处的位置是
a
a
(填“a”或“b”).

②图二中,能够检验二氧化碳是否收集满的方法是
Ⅱ
Ⅱ
.
③该发生装置不具有启普发生装置的原理,理由是
Ⅱ
Ⅱ
.
Ⅰ.不能控制反应的发生
Ⅱ.不能控制反应的停止
Ⅲ.不能控制反应的发生和停止
实验三:计算实验室使用的大理石中碳酸钙的质量分数用足量的盐酸与12g块状大理石反应,得到0.1mol二氧化碳(杂质不参加反应).
④求块状大理石中碳酸钙的质量.(请根据化学方程式计算)
⑤该大理石中碳酸钙的质量分数是
83.3%
83.3%
(精确到0.1%).







 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案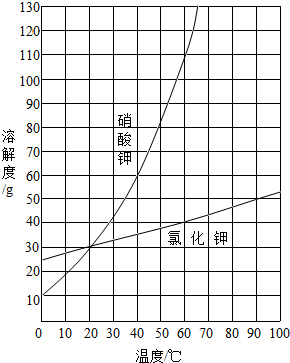 (2012?虹口区一模)如图是氯化钾和硝酸钾的溶解度曲线,回答以下问题.
(2012?虹口区一模)如图是氯化钾和硝酸钾的溶解度曲线,回答以下问题.