氢氧化钠(NaOH)和氢氧化钙[Ca(OH)2]是常见的碱,在现实生活中有广泛的用途。根据所学知识回答:
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是________。
(2)实验室常用澄清的石灰水来检验二氧化碳,将饱和的石灰水溶液升高温度,溶液浓度将________(填“增大”、“减小”或“不变”)。
(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,反应的化学方程式是________。
(4)农业生产中常用氢氧化钙和硫酸铜配置波尔多液来防治果树的霉叶病等,配制波尔多液时________(填“能”或“不能”)用铁制容器。
(5)氢氧化钠常用来干燥某些气体,其干燥原理是________。
CO32— 减小 H2SO4 +Ca(OH)2 = CaSO4 + 2H2O 不能 能吸收气体中的水分表面形成溶液。(合理即可)。
(1)氢氧化钠极易吸收水分而潮解并和空气中的二氧化碳反应生成碳酸钠和水而变质,最终生成碳酸钠
(2)由于氢氧化钙的溶解度随温度的升高而减小,因此将氢氧化钙的饱和溶液升高,溶液中就会有晶体析出,因此溶液中的溶质就会减少,则溶液浓度将减小
(3)氢氧化钙显碱性,能与酸发生中和反应,可用于改良酸性土壤, 反应的化学方程式是H2SO4 +Ca(OH)2 = CaSO4 + 2H2O
(4)在金属活动性顺序中,铁在铜的前面,能与硫酸铜反应生成硫酸亚铁和铜,使药效降低,故不能使用铁制容器;
(5)固体氢氧化钠常用作干燥剂是因为它能在空气中吸收水分而在其表面形成溶液



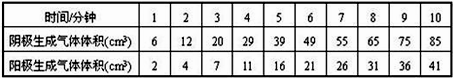
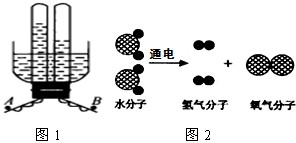 如图1是某同学自己设计的装置:用大塑料瓶子截去瓶底,留瓶口一段约8cm~10cm,瓶口配一胶塞由里往外塞紧.A、B两极是用镀铬曲别针伸直做成,由塞子露头处连接导线.试回答:
如图1是某同学自己设计的装置:用大塑料瓶子截去瓶底,留瓶口一段约8cm~10cm,瓶口配一胶塞由里往外塞紧.A、B两极是用镀铬曲别针伸直做成,由塞子露头处连接导线.试回答: