
| ʵ����� | �������������/% | ��Ӧ�¶�/�� | ��˿��ʧ��ʱ��/s |
| �� | 3 | 20 | 500 |
| �� | 6 | 20 | 300 |
| �� | 6 | 30 | 80 |
���� ��1������������������ķ�Ӧ��
��2���ȽϢں͢ۿ��Կ������ǵIJ�֮ͬ���������¶ȣ�
��3���ں͢�������Ũ����ȣ����ܱ�������Ũ�ȶԷ�ӦӰ����Ǣٺ͢ڣ�
��4��������Ũ�ȸ�Ϊ4%��ô��ʱŨ����3%��6%֮�䣬���Է�Ӧ����ʱ��ҲӦ������֮�䣻
���㷴Ӧ�����ķ����ܶ࣬���������ͬ��������������ʱ�䳤�̡��������ݵĿ����ȶ��ܹ�������Ӧ������
��� �⣺��1���������ᷴӦ���û���Ӧ��Ҫ�����������ʱ����Ϊ��2Al+6HCl=2AlCl3+3H2����
��2����������Ũ��Ϊ6%�¶�Ϊ20�棬��������Ũ��Ϊ6%�¶�Ϊ30�棬���Կ���������ʱ��϶̣��Ӷ������ж��¶Ȳ�ͬ����ʱ��Ҳ��ͬ���ʱ����Ϊ���¶ȣ�
��3���ȽϢٺ͢��е����ݿ�֪Ũ��Խ��Ӧ����ʱ��Խ�̣��ʱ����Ϊ���٢ڣ�
��4��Ũ��Ϊ3%����ʱ��Ϊ500�룬Ũ��Ϊ6%����ʱ��Ϊ300�룬��ô��Ũ��Ϊ4%ʱ������ʱ��Ӧ����300����500��֮�䣻
�ж�һ����Ӧ�Ŀ����ж��ַ���������������Ŀ���ͨ���������ݵĿ������жϷ�Ӧ�Ŀ�����������ͨ���¶����ߵĿ������жϵȣ��ʱ����Ϊ��300��t��500������ˮ���ռ�һƿ��������ʱ��Ķ�������������ͨ����λʱ�������������������¶ȱ仯�������ȣ����������𰸾��ɣ���
���� ������ͨ�����Ʋ�ͬ������̽���ܹ�Ӱ�췴Ӧ�ٶȵ����صģ�����������������ѧ�Ŀ��Ʊ�������������⣬�����ڽ��ʱҪע����ϸ�����Ƚϣ��Ӷ��ó���ȷ�Ľ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ���Ĵ�ʡ2017����꼶�п���Ӧ�Կ��������ۺϻ�ѧ�Ծ� ���ͣ������
��1��ͼ����þԭ�Ӻ���ԭ���γ�����þ��ʾ��ͼ
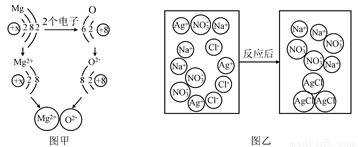
�ٴӵ�ʧ���ĽǶȿ���þ�������ķ�Ӧ����____ ��Ӧ���ӵ�ʧ���ӵĽǶȿ�����Ӧ��þԭ��______����õ�����ʧȥ����2�����ӣ��γ�����ȶ��ṹ��
����ͼ��֪��Ԫ�ص�ԭ�ӵõ����Ӻ��仯�ϼ۽�______������ߡ����͡�����
��2��ͼ����NaCl��AgNO3����Һ��Ӧ��ʾ��ͼ��
��ͼ��NO3����������______________ ��
�ڸ÷�Ӧ�ı�����__________________������ɳ�����
��������AgNO3����Ӧ��֮һ��д����һ����������Ӧ������ͬ�Ļ�ѧ����ʽ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���д��������꼶��ѧ��һģ��ѧ�Ծ��������棩 ���ͣ�ѡ�������
��һ������̼�����ƺ��Ȼ��ƵĻ����Һ�м���ϡ������Һ��������ij���� y��x�ı仯��������ͼ��ʾ����x��ʾϡ�������������y��ʾ�ĺ�����

A. �Ȼ��Ƶ����� B. ��Һ��������
C. ������̼������ D. ��Һ����Ԫ�ص�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���д��������꼶��ѧ��һģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���������У�������Һ����
A��ţ�� B������ C����ˮ D����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��㶫ʡ��ͷ�����������꼶�п�ģ�⻯ѧ�Ծ��������棩 ���ͣ������
�Ժ�п����(��Ҫ�ɷ�ΪZnO������ΪFeO��CuO)Ϊԭ���Ʊ���ˮ����п(ZnSO4•7H2O)��������ͼ��

(1)�����Ŀ����_________��
(2)����X��______�������к��н���������______����ͭʱ�����ķ�Ӧ����ʽΪ______��
(3)�����л����ˮ����пǰʡ�ԵIJ�����______����ȴ�ᾧ��_____��ϴ�Ӻ͵��º�ɣ�
a�������ᾧ b������Ũ�� c����ˮϡ�� d������
(4)ij�¶��£�Fe(OH)3�ֽ�õ�һ��������������Ϊ21��8���������������Ļ�ѧʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | 1 | 2 | 3 | 4 | 5 | |
| ����״̬ | ˿״ | ��ĩ״ | ˿״ | ˿״ | ˿״ | |
| ϡ������������/% | 5 | 5 | 10 | 10 | 15 | |
| ��Һ�¶�/�� | ��Ӧǰ | 20 | 20 | 20 | 35 | ��ʧ���� |
| ��Ӧ�� | 34 | 35 | 35 | 50 | 55 | |
| ������ʧ��ʱ��/s | 500 | 50 | 125 | 50 | 30 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ǰ���пƴ����ܽ����о���ɹ��ϳ��˲�ͬ�ߴ硢��������˫���εIJ�ͭ˫�����༶�ṹ��������ͼ��ͭ�Ͳ������ڱ��е���Ϣ������˵��������ǣ�������
��ǰ���пƴ����ܽ����о���ɹ��ϳ��˲�ͬ�ߴ硢��������˫���εIJ�ͭ˫�����༶�ṹ��������ͼ��ͭ�Ͳ������ڱ��е���Ϣ������˵��������ǣ�������| A�� | ͭԭ�ӵĺ˵������29 | B�� | ����Ԫ�ط�����Pt | ||
| C�� | ͭ�Ļ�ԱȲ�ǿ | D�� | �������ԭ������Ϊ195.1g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com