


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源:不详 题型:单选题
| 需鉴别的物质 | 所加试剂及方法 | ||
| 方法1 | 方法2 | ||
| A | 木炭粉和氧化铜 | 加水观察是否溶解 | 通CO并加热 |
| B | 氢氧化钠溶液和碳酸钠溶液 | 稀盐酸 | 无色酚酞试液 |
| C | CO和CO2 | 闻气味 | 澄清石灰水 |
| D | 稀盐酸和氯化钠溶液 | Fe | pH试纸 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.称量时,将粗盐放在天平右盘的称量纸上 |
| B.蒸发操作中,玻璃棒的主要作用是防止液滴飞溅 |
| C.主要操作步骤是:计算、称量、量取、溶解 |
| D.过滤时用到的主要仪器、用品是:玻璃棒、烧杯、滤纸、铁架台 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | Cu( CuO) | 加足量盐酸后过滤 |
| B | H2(HCl) | 通过足量 Na2CO3溶液 |
| C | CaO(CaCO3) | 加水、过滤、蒸发 |
| D | NaCl(CuCl2) | 加过量NaOH溶液后过滤 |
查看答案和解析>>
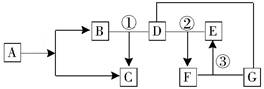
科目:初中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| | 物质 | 所含杂质 | 除去杂质的试剂或方法 |
| A | Na2C03固体 | NaHC03固体 | 加热 |
| B | Cu | Fe | 加过量稀盐酸后过滤、洗涤、干燥 |
| C | 02 | H20 | 通人盛有过量浓H2S04的洗气瓶 |
| D | C02 | HC1 | 通入盛有NaOH溶液的洗气瓶,然后干燥 |
查看答案和解析>>
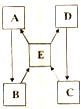
科目:初中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| | 物质 | 所含杂质 | 除去杂质的方法 |
| A | NaCl溶液 | Na2C03 | 加入稀硫酸至不再产生气泡 |
| B | N2气体 | 02 | 将气体缓缓通过灼热的铜网 |
| C | Cu0粉末 | C | 加入过量稀盐酸,充分反应 |
| D | KCl溶液 | CuCl2 | 加入NaOH溶液至不再产生沉淀 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
| 反应物Ⅰ | 反应物Ⅱ | 反应现象 | 说 明 |
| AgNO3溶液 | NaCl溶液 | 生成白色沉淀 | 该沉淀为AgCl,不溶于稀硝酸 |
| BaCl2溶液 | Na2SO4溶液 | 生成白色沉淀 | 该沉淀为BaSO4,不溶于稀硝酸 |
| Na2CO3溶液 | | 生成白色沉淀 | 该沉淀为 ,溶于稀盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com